Все работы по биосинтезу флавоноидов подтвердили, что флоро— глюциновое ядро А образуется по ацетатному механизму - конденсацией трех молекул уксусной кислоты. Предполагается участие аце— тилкофермента А или малонилкофермента А. Циклизация остатка Р-поликетокислоты приводит к образованию не идентифицированных до настоящего времени промежуточных продуктов. Наиболее правдоподобно, что фенольные гидроксилы в положениях 5 и 7 происходят от карбоксильных групп молекул уксусной кислоты.[ ...]
Вторая часть молекулы флавоноидов — фенилпропановая (цикл В) — происходит от фенилаланина. При радиоизотопных исследованиях биосинтеза флавоноидов всегда обнаруживалось, что шикимовая кислота вступала в молекулу флавоноида; тем самым обосновывается взгляд, что биогенетический путь образования этой части молекулы протекает через шикимовую и префеновую кислоты с образованием фенилаланина и производных коричной кислоты, которые по всей вероятности, присоединяют триацетатное производное, образуя промежуточный халкон. Гидроксилирование в цикле В происходит уже на уровне продукта С9» и следует полагать, что возникает гидроксилированная коричная кислота.[ ...]
Сходство биогенезиса флавонов, флаванов, антоцианинов позволяет прийти к заключению, что растительные флавоноиды образуются по одинаковому биогенетическому механизму.[ ...]
Фенольные соединения считаются вторичными метаболитами в растениях. Они образуются из первичных метаболитов - углеводов — по двум основным механизмам, описанным в этой главе. Ацетатный механизм приводит к образованию фенольных соединений преимущественно в низших растениях, механизм же с участием шикимовой кислоты относится главным образом к высшим растениям. Нередко оба эти пути биосинтеза фенольных соединений объединяются, как, например, при образовании флавоноидов.[ ...]
Значительную роль при ароматизации ациклических соединений играют фенилпир овин оградные кислоты - как первичные ароматические продукты - и ароматические аминокислоты - фенилаланин и тирозин. Для этих аминокислот характерны два типа реакций - декар-боксилирование, ведущее к образованию алкалоидов, и дезаминирование, приводящее к коричной кислоте и ее производным, из которых далее образуются многие растительные фенольные соединения, как схематически изображено на рис. 11.[ ...]
Рисунки к данной главе:
| Биосинтез флавоноидов по Робинсону- |
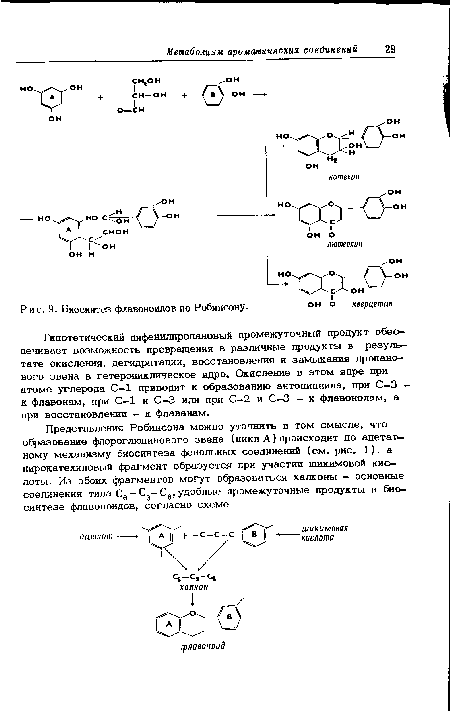 |
| Биосинтез катехинов. |
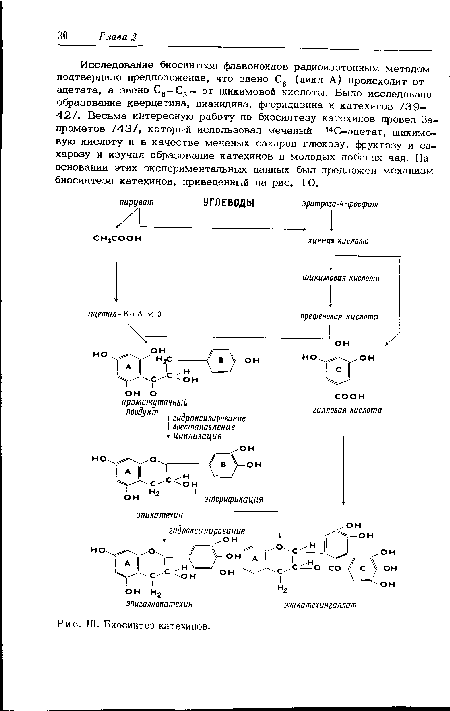 |
| Биогенетическая связь растительных фенольных соединений. |
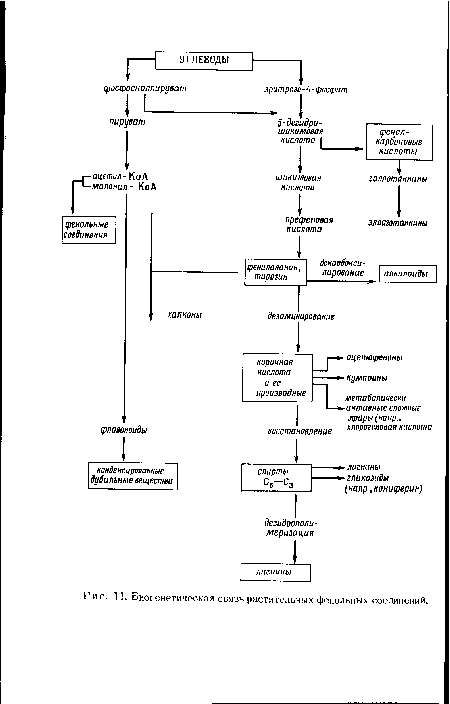 |