| Нормальные моды колебания Н20 [239]. |
![Нормальные моды колебания Н20 [239].](/static/pngsmall/318624928.png) |
Далее
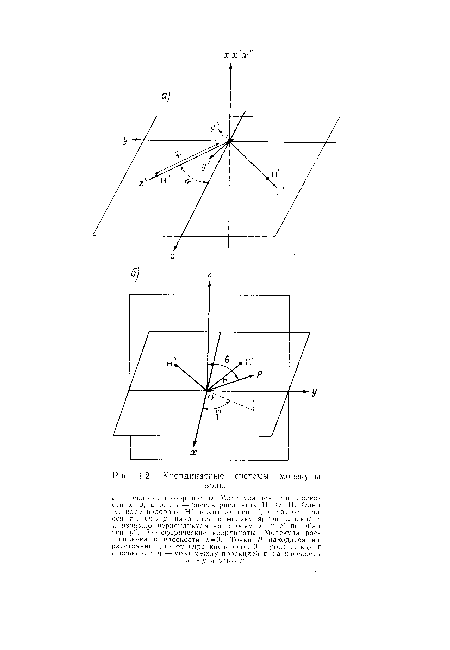
| Координатные системы молекулы |
 |
Далее
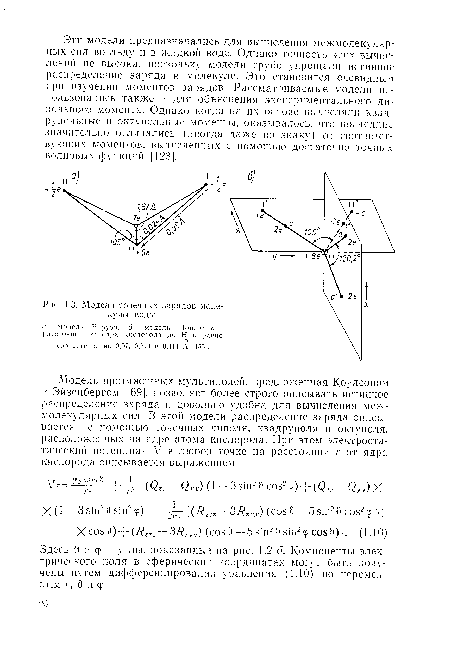
| Модели точечных зарядов молекулы воды. |
 |
Далее
| Образование системы связывающих м. о. из 2р-орби-талей атома кислорода и ^-орбитали атома водорода [(¡7]. |
![Образование системы связывающих м. о. из 2р-орби-талей атома кислорода и ^-орбитали атома водорода [(¡7].](/static/pngsmall/318624960.png) |
Далее
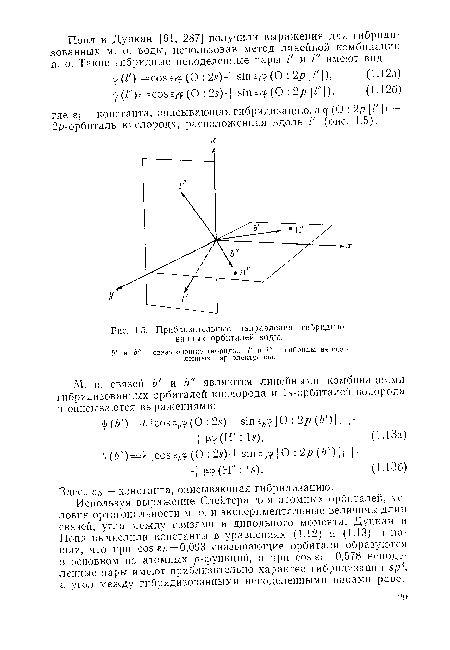
| Приблизительные направления гибрндизо-ванных орбиталей воды. |
 |
Далее
| Контурная карта электронной плотности, пока зывгюшая плотность валентных электронов в молекулярной плоскости для волновой функции почти идентичной волновой функции Дункана и Попла. Плотности даются в атомных единицах [8]. |
![Контурная карта электронной плотности, пока зывгюшая плотность валентных электронов в молекулярной плоскости для волновой функции почти идентичной волновой функции Дункана и Попла. Плотности даются в атомных единицах [8].](/static/pngsmall/318624964.png) |
Далее
| Связывающая область молекулы воды, согласно Бадеру [6]. Пунктирные линии отделяют связывающую область (заштрихованную) от антисвязывающен области. |
![Связывающая область молекулы воды, согласно Бадеру [6]. Пунктирные линии отделяют связывающую область (заштрихованную) от антисвязывающен области.](/static/pngsmall/318624968.png) |
Далее
| Диаграммы Ар для бадеровского распределения заряда с изогнутыми связями (см. текст) [6]. Значения Др нанесены в атомных единицах • 100. |
![Диаграммы Ар для бадеровского распределения заряда с изогнутыми связями (см. текст) [6]. Значения Др нанесены в атомных единицах • 100.](/static/pngsmall/318624970.png) |
Далее
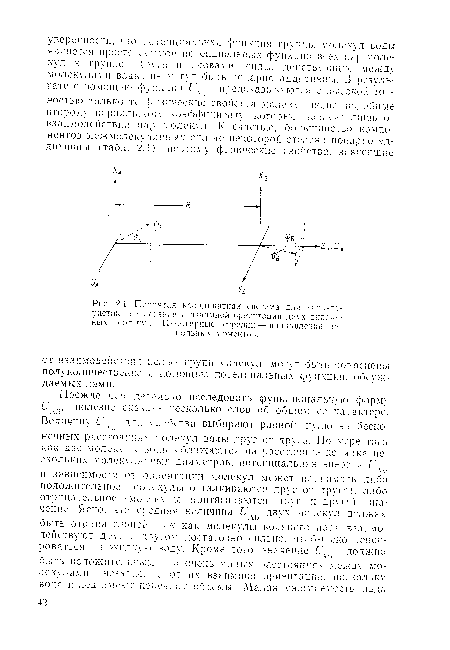
| Принятая координатная система для характеристик |
 |
Далее
| Потенциальная энергия взаимодействия двух молекул воды, имеющих фиксированные взаимные ориентации в соответствии с потенциалом Штокмайера [уравнение (2.17)]. |
![Потенциальная энергия взаимодействия двух молекул воды, имеющих фиксированные взаимные ориентации в соответствии с потенциалом Штокмайера [уравнение (2.17)].](/static/pngsmall/318624992.png) |
Далее
| Взаимные ориентации двух молекул воды, энергии взаимодействия которых даны в табл. 2.2. |
 |
Далее
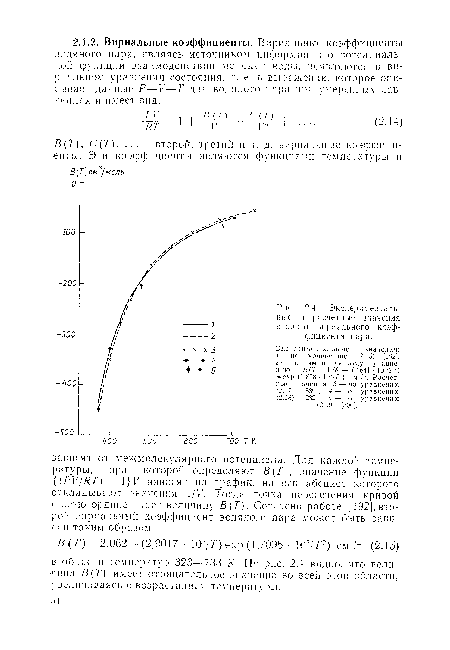
| Экспериментальные п расчетные значения второго вирнального коэффициента пара. |
 |
Далее
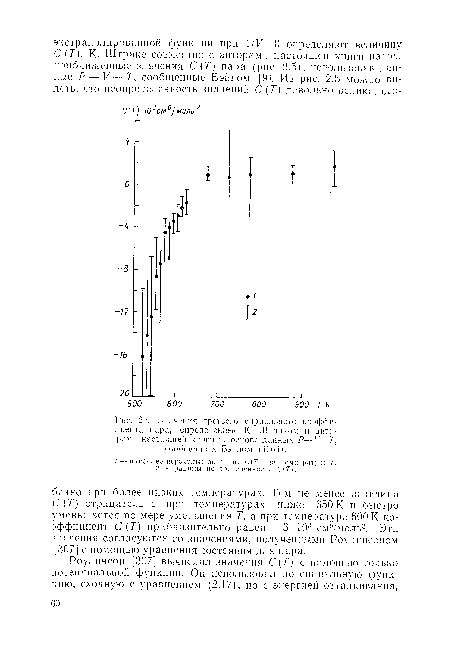
| Значения третьего иирнального коэффициента пара, определенные К. Штарком и авторами настоящей книги на основе данных Р—V—Г, сообщенных Бэпно.м (1964). |
 |
Далее
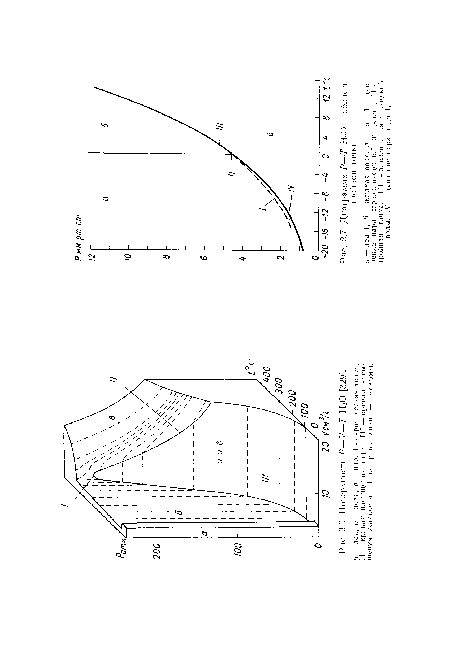
| Диаграмма Р—Т Н20 н области тронной точки. |
 |
Далее
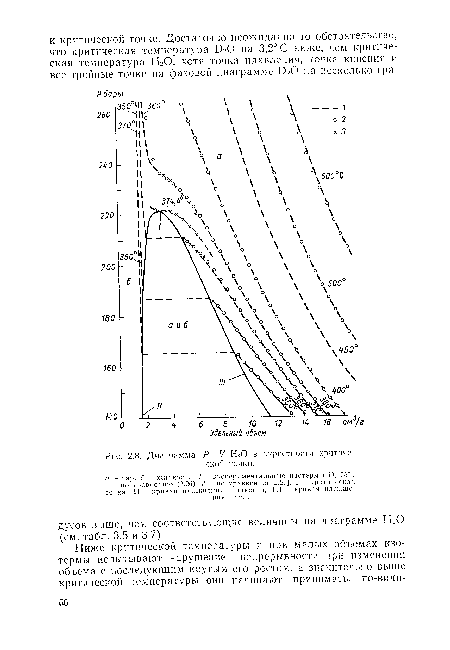
| Диаграмма Р—V Н20 в окрестности критической точки. |
 |
Далее
| Энтропия воды как функция температуры и давления [329]. Липни постоянного давления приведены на поверхности. |
![Энтропия воды как функция температуры и давления [329]. Липни постоянного давления приведены на поверхности.](/static/pngsmall/318625046.png) |
Далее
| Удельная теплота Н20 при атмосферном давлении [393]. Удельная теплота пара вместе с критической изобарой стремится к бесконечности по мерс того, как температура понижается, приближаясь к критической. |
![Удельная теплота Н20 при атмосферном давлении [393]. Удельная теплота пара вместе с критической изобарой стремится к бесконечности по мерс того, как температура понижается, приближаясь к критической.](/static/pngsmall/318625048.png) |
Далее
| Изображение кристалла льда I, показывающее Е!аидерваальсовы радиусы атомов [280]. Вид снизу вдоль оси с, показывающий наличие открытых «каналов». |
![Изображение кристалла льда I, показывающее Е!аидерваальсовы радиусы атомов [280]. Вид снизу вдоль оси с, показывающий наличие открытых «каналов».](/static/pngsmall/318625056.png) |
Далее
| Молекулярные параметры льда I из D2O при —50° С, определенные Петерсоном н Леви [279]. В любой данный момент времени имеется только один дейтрон вдоль каждой линии О ... О. Точность определения параметров, вероятно, ниже, чем точность, с которой приведены значения па рисунке (ем. [223]). Воспроизведено из работы Оустона [269]. |
![Молекулярные параметры льда I из D2O при —50° С, определенные Петерсоном н Леви [279]. В любой данный момент времени имеется только один дейтрон вдоль каждой линии О ... О. Точность определения параметров, вероятно, ниже, чем точность, с которой приведены значения па рисунке (ем. [223]). Воспроизведено из работы Оустона [269].](/static/pngsmall/318625060.png) |
Далее
| Структура льда III, показанная вдоль осп с [174]. Атомы кислорода изображены в виде кружков, а связи О—Н ... О — в виде стержней, атомы водорода не показаны. Цифры, стоянию v атомов кислорода, дают нх г-коордппаты в сотых долях длины осп с. Цифры около связей выражают их длины в А. Атомы 0| и 02 рассматриваются в тексте. |
![Структура льда III, показанная вдоль осп с [174]. Атомы кислорода изображены в виде кружков, а связи О—Н ... О — в виде стержней, атомы водорода не показаны. Цифры, стоянию v атомов кислорода, дают нх г-коордппаты в сотых долях длины осп с. Цифры около связей выражают их длины в А. Атомы 0| и 02 рассматриваются в тексте.](/static/pngsmall/318625080.png) |
Далее
| Структура льда V, показанная вдоль оси b [178]. Атомы кислорода изображены в виде кружков, а связи О—Н ... О — в виде стержней; атомы водорода не показаны. Цифры рядом с атомами кислорода характеризуют их К-координаты в сотых долях длины оси Ь (7,54 А). Цифры около связей дают их длины в А. Пронумерованные молекулы обсуждаются в тексте [178]. |
![Структура льда V, показанная вдоль оси b [178]. Атомы кислорода изображены в виде кружков, а связи О—Н ... О — в виде стержней; атомы водорода не показаны. Цифры рядом с атомами кислорода характеризуют их К-координаты в сотых долях длины оси Ь (7,54 А). Цифры около связей дают их длины в А. Пронумерованные молекулы обсуждаются в тексте [178].](/static/pngsmall/318625082.png) |
Далее
| Структура льда VI [172]. Молекулы воды изображены здесь таким же образом, как и на рис. 3.7. |
![Структура льда VI [172]. Молекулы воды изображены здесь таким же образом, как и на рис. 3.7.](/static/pngsmall/318625086.png) |
Далее
| Структура льдов VII и VIII [177]. Водородные связи показаны в виде точечных линий, а единичная ячейка изображена сплошными линиями. Молекулы воды показаны в одном из многих наборов ориентаций, которые они, по-видимому, имеют во льду VII. Во льду VIII их ориентации упорядочены, однако природа этой упорядоченности еще не известна. Вполне вероятно, что при упорядоченном расположении молекулы одной решетки имеют благоприятные условия для электростатических взаимодействии с молекулами другой решетки. |
![Структура льдов VII и VIII [177]. Водородные связи показаны в виде точечных линий, а единичная ячейка изображена сплошными линиями. Молекулы воды показаны в одном из многих наборов ориентаций, которые они, по-видимому, имеют во льду VII. Во льду VIII их ориентации упорядочены, однако природа этой упорядоченности еще не известна. Вполне вероятно, что при упорядоченном расположении молекулы одной решетки имеют благоприятные условия для электростатических взаимодействии с молекулами другой решетки.](/static/pngsmall/318625088.png) |
Далее
| Расположение атомов кислорода во льду 1с [45]. Это расположение изоморфно с расположением атомов в алмазе. Единичная ячейка изображена пунктирными линиями. |
![Расположение атомов кислорода во льду 1с [45]. Это расположение изоморфно с расположением атомов в алмазе. Единичная ячейка изображена пунктирными линиями.](/static/pngsmall/318625092.png) |
Далее
| Теплоемкость в кал/(моль • °С) (/), энтропия в кал/(моль • СС) (2), энтальпия в ккал/моль (3) и свободная энергия Гиббса в ккал/моль (4) Н20 при давлении 1 атм [86]. |
![Теплоемкость в кал/(моль • °С) (/), энтропия в кал/(моль • СС) (2), энтальпия в ккал/моль (3) и свободная энергия Гиббса в ккал/моль (4) Н20 при давлении 1 атм [86].](/static/pngsmall/318625106.png) |
Далее
| Статическая диэлектри- ческая постоянная льда I (е0) как функция температуры. х |
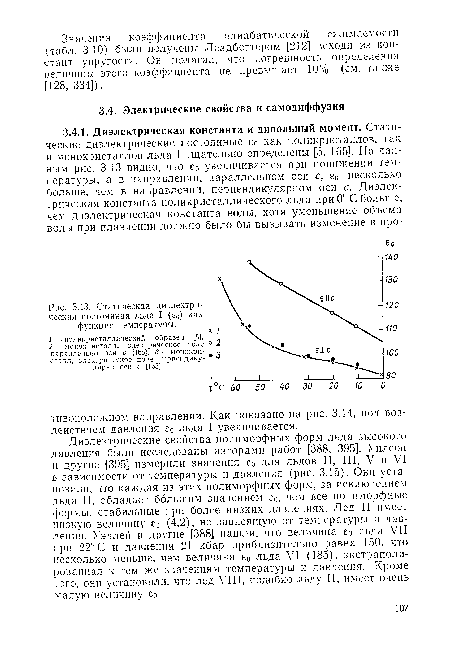 |
Далее
| Величина дипольного момента т молекулы Н,0 во льду больше, чем соответствующая величина для изолированной молекулы воды |л, из-за электростатических полей, создаваемых дипольными моментами соседних молекул. Здесь показана произвольная центральная молекула с четырьмя ее ближайшими соседями. Электростатическое поле Р, обусловленное соседями, наводит добавочный момент иР у центральной молекулы. |
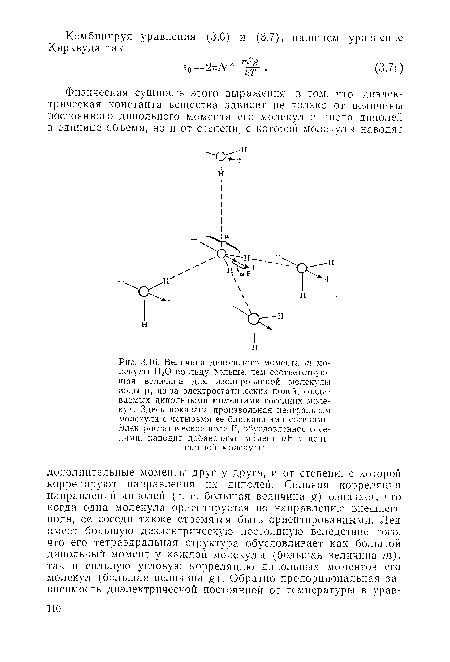 |
Далее
| Схематическое изображение образования пары Д- и ¿-дефектов во льду I. Ось с перпендикулярна плоскости рисунка. |
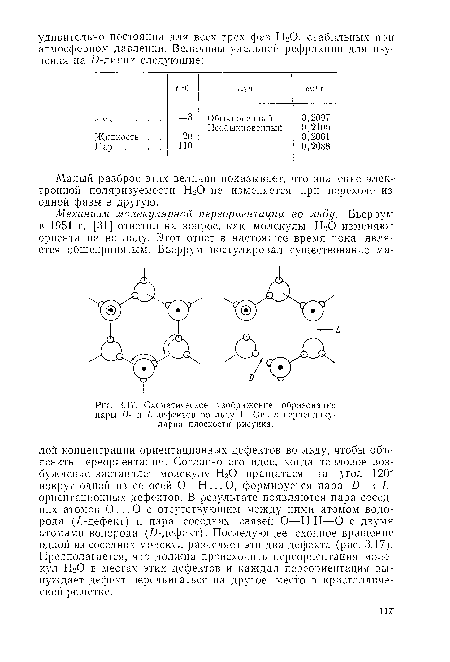 |
Далее
| Схематическое изображение образования и миграции иопньгх дефектов во льду I. |
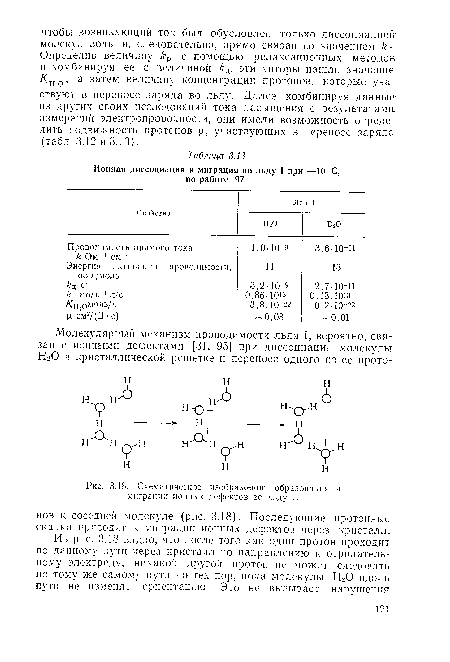 |
Далее
| Равновесные размеры молекулы воды во льду I [206]. Заштрихованная полоса показывает значения, согласующиеся со спектром ЯМР льда I, полученным Куме [206]. Значения а и б предложены соответственно Петерсоном и Леви [279] и Чидамбарамом [57] на основании исследований фракции нейтронов льда I из 020. |
![Равновесные размеры молекулы воды во льду I [206]. Заштрихованная полоса показывает значения, согласующиеся со спектром ЯМР льда I, полученным Куме [206]. Значения а и б предложены соответственно Петерсоном и Леви [279] и Чидамбарамом [57] на основании исследований фракции нейтронов льда I из 020.](/static/pngsmall/318625186.png) |
Далее
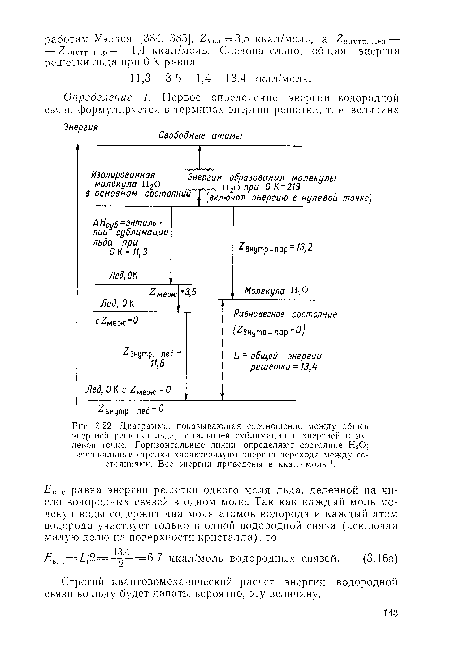
| Диаграмма, показывающая соотношение между общей энергией решетки льда, энтальпией сублимации и энергией в нулевой точке. Горизонтальные линии определяют состояние НгО; вертикальные стрелки характеризуют энергии перехода между состояниями. Все энергии приведены в ккал • моль-1. |
 |
Далее
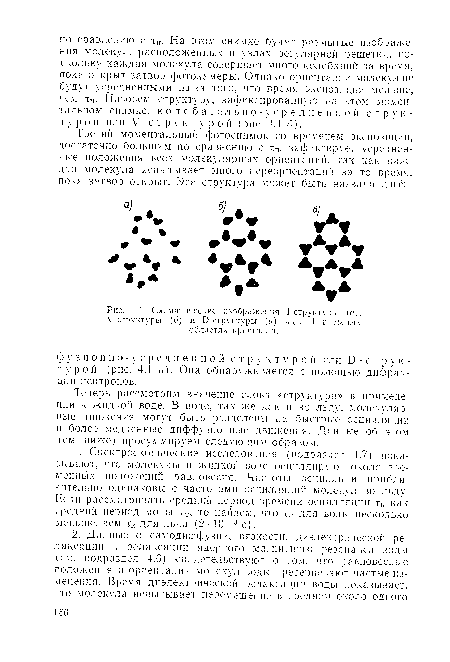
| Схематические изображения 1-структуры (а), -структуры (б) и В-структуры (а) льда 1 в малых областях кристалла. |
 |
Далее
| Временной масштаб молекулярных процессов во льду и жидкой |
 |
Далее
| Радиальные функции распределения g (f?) жидкой Н20 при различных температурах и жидкой D20 при 4° С [251]. Отметим, что базисная линия каждой кривой на одну единицу выше базисной линии кривой, расположенной ниже. Сплошные кривые были вычислены с помощью модели, которая описана и п. 4.2.2. Эксперименты при 100° С и ниже выполнены при атмосферном давлении, эксперименты при температурах выше 100° С проводились при давлении пара образца. |
![Радиальные функции распределения g (f?) жидкой Н20 при различных температурах и жидкой D20 при 4° С [251]. Отметим, что базисная линия каждой кривой на одну единицу выше базисной линии кривой, расположенной ниже. Сплошные кривые были вычислены с помощью модели, которая описана и п. 4.2.2. Эксперименты при 100° С и ниже выполнены при атмосферном давлении, эксперименты при температурах выше 100° С проводились при давлении пара образца.](/static/pngsmall/318625226.png) |
Далее
| Радиальные функции распределения АпИ2р(Д) жидкой Н20 при различных температурах и жидкой 020 при 4° С [250]. |
![Радиальные функции распределения АпИ2р(Д) жидкой Н20 при различных температурах и жидкой 020 при 4° С [250].](/static/pngsmall/318625228.png) |
Далее
| Интерпретация радиальных кривых распределения воды на основе смешанной модели Немети и Шерага [252]. |
![Интерпретация радиальных кривых распределения воды на основе смешанной модели Немети и Шерага [252].](/static/pngsmall/318625238.png) |
Далее
| Вклады в радиальную функцию распределения воды, вычисленные Поплом [288]. |
![Вклады в радиальную функцию распределения воды, вычисленные Поплом [288].](/static/pngsmall/318625248.png) |
Далее
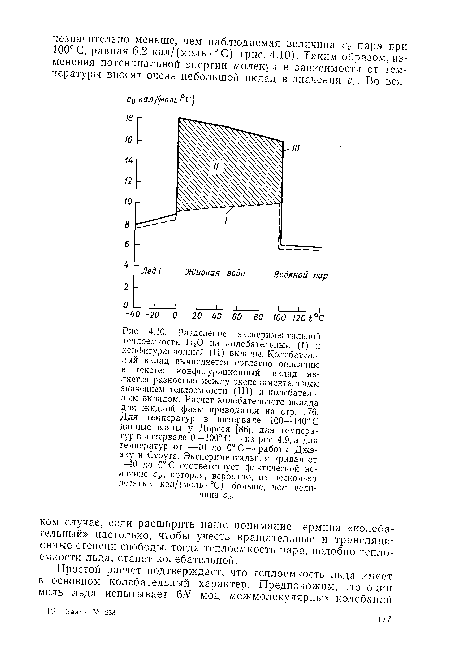
| Разделение экспериментальной теплоемкости Н20 на колебательный (I) и конфигурационный (II) вклады. Колебательный вклад вычисляется согласно описанию в тексте; конфигурационный вклад является разностью между экспериментальным значением теплоемкости (III) и колебательным вкладом. Расчет колебательного вклада для жидкой фазы приводится на стр. 176. |
 |
Далее
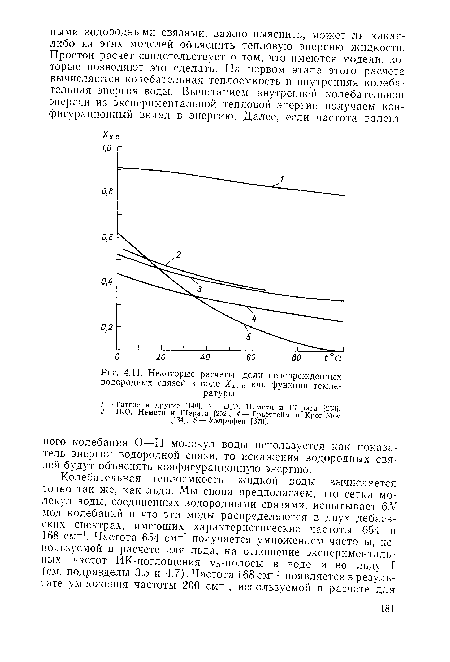
| Некоторые расчеты доли неповрежденных водородных связей в воде Хв. 0 как функции температуры. |
 |
Далее
| Разделение наблюдаемой тепловой энергии волы на колебательный (/) и конфигурационный (//) вклады. Колебательный вклад был вычислен согласно описанию в тексте, а конфигурационный вклад— вычитанием колебательной энергии из наблюдаемой тепловой энергии. Спектроскопические данные для льда п жидкой воды получены Фалком и Фордом [104] и Бенедиктом и другими [19]. ///—экспериментальная энергия. 1—конфигурационная энергия, вычисленная с помощью уравнения (4.5) и экспериментальной валентной частоты связи О—Н. Валентная частота О—Н жидкой воды при 0° С вычислена путем экстраполяции данных Фалка и Фонда. |
![Разделение наблюдаемой тепловой энергии волы на колебательный (/) и конфигурационный (//) вклады. Колебательный вклад был вычислен согласно описанию в тексте, а конфигурационный вклад— вычитанием колебательной энергии из наблюдаемой тепловой энергии. Спектроскопические данные для льда п жидкой воды получены Фалком и Фордом [104] и Бенедиктом и другими [19]. ///—экспериментальная энергия. 1—конфигурационная энергия, вычисленная с помощью уравнения (4.5) и экспериментальной валентной частоты связи О—Н. Валентная частота О—Н жидкой воды при 0° С вычислена путем экстраполяции данных Фалка и Фонда.](/static/pngsmall/318625268.png) |
Далее
| Молярные объемы льда I из Н20 и четырех изотопов жидкой воды при давлении 1 атм. Вставка — увеличенное изображение кривой для жидкой НгО в интервале температур от —4 до 12° С. Данные для льда I взяты из табл. 3.10. Кривые для жидкости вычислялись с помощью уравнения (4.6). Использовались следующие значения молекулярного веса |
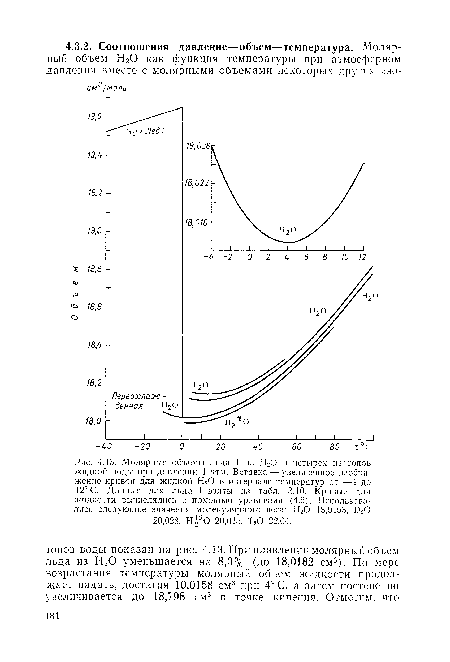 |
Далее
| Коэффициент теплового расширения при постоянном давлении ß льда I и жидкой воды при давлении 1 атм. Заштрихован участок отрицательных значений ß. Ось температуры сокращена ниже 0°С. Данные для льда I взяты из табл. 3.10 и из работы [75], а для жидкой воды — из обзора [185]. |
![Коэффициент теплового расширения при постоянном давлении ß льда I и жидкой воды при давлении 1 атм. Заштрихован участок отрицательных значений ß. Ось температуры сокращена ниже 0°С. Данные для льда I взяты из табл. 3.10 и из работы [75], а для жидкой воды — из обзора [185].](/static/pngsmall/318625274.png) |
Далее
| Коэффициент изотермической сжимаемости ут жидкой воды при давлении 1 агм [185]. |
![Коэффициент изотермической сжимаемости ут жидкой воды при давлении 1 агм [185].](/static/pngsmall/318625276.png) |
Далее
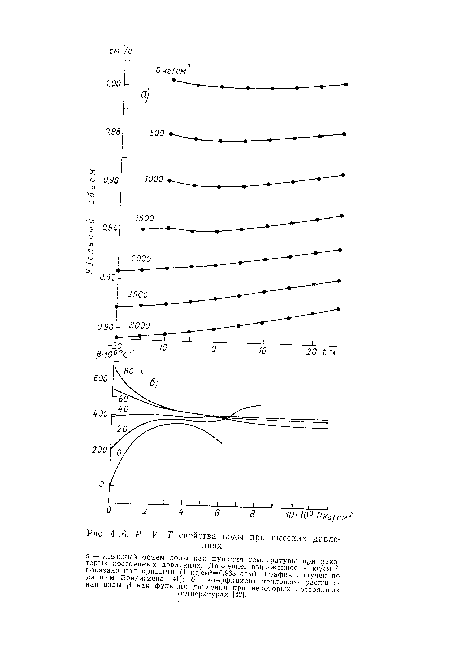
| Рис. 4.16. Р—V—Т свойства воды при высоких давлениях. |
 |
Далее
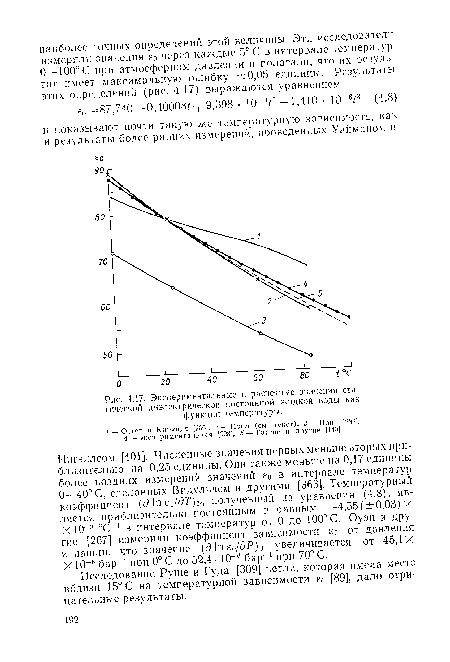
| Экспериментальные и расчетные значения статической диэлектрической постоянной жидкой воды как функции температуры. |
 |
Далее
| Показатель преломления п жидкой воды в инфракрасной области спектра [196]. |
![Показатель преломления п жидкой воды в инфракрасной области спектра [196].](/static/pngsmall/318625308.png) |
Далее
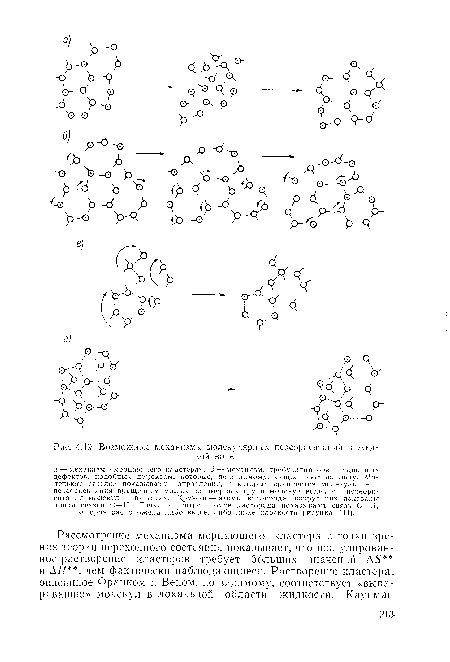
| Возможные механизмы молекулярных переориентации в жидкой воде. |
 |
Далее
| Среднее квадратичное перемещение (/?2) протона в жидкой воде как функция времени [311]. |
![Среднее квадратичное перемещение (/?2) протона в жидкой воде как функция времени [311].](/static/pngsmall/318625350.png) |
Далее
| Зависимость вязкости сдвига воды от давления, согласно Бетту и Чаппи [29]. |
![Зависимость вязкости сдвига воды от давления, согласно Бетту и Чаппи [29].](/static/pngsmall/318625354.png) |
Далее
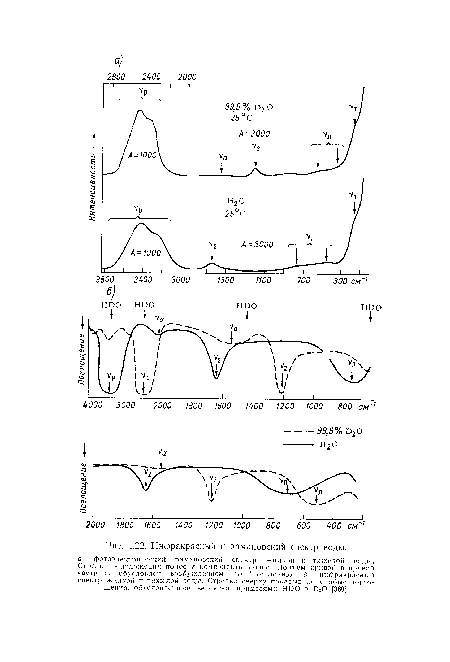
| Инфракрасный и рамановский спектр воды. |
 |
Далее
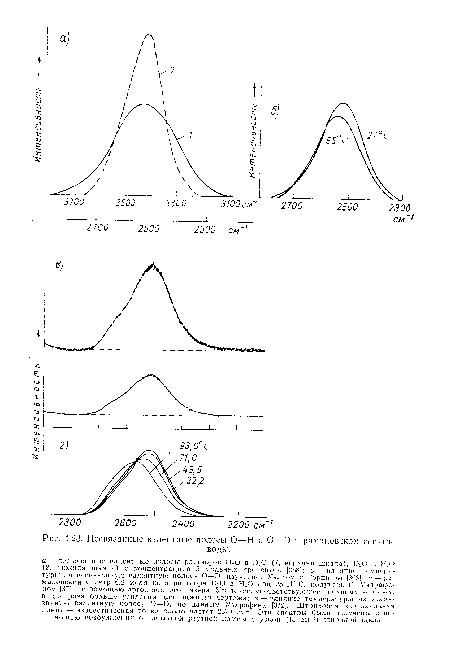
| Несвязанные валентные полосы О—Н и О—О в римановском спектре |
 |
Далее
| Распределение расстояний до ближай-ших соседей в жидкой воде, полученное согласно форме несвязанных валентных полос [368]. Ордината кривой па любом данном расстоянии пропорциональна доле молекул, имеющих ближайшего соседа на этом расстоянии. |
![Распределение расстояний до ближай-ших соседей в жидкой воде, полученное согласно форме несвязанных валентных полос [368]. Ордината кривой па любом данном расстоянии пропорциональна доле молекул, имеющих ближайшего соседа на этом расстоянии.](/static/pngsmall/318625386.png) |
Далее
| Структура из пяти молекул воды, соединенных водородными связями, использованная Уэлрафеном [369] для отнесения межмолекулярных полос воды к нормальным колебаниям. |
![Структура из пяти молекул воды, соединенных водородными связями, использованная Уэлрафеном [369] для отнесения межмолекулярных полос воды к нормальным колебаниям.](/static/pngsmall/318625400.png) |
Далее
| Вращение молекулы H2O в жидкой воде. |
 |
Далее
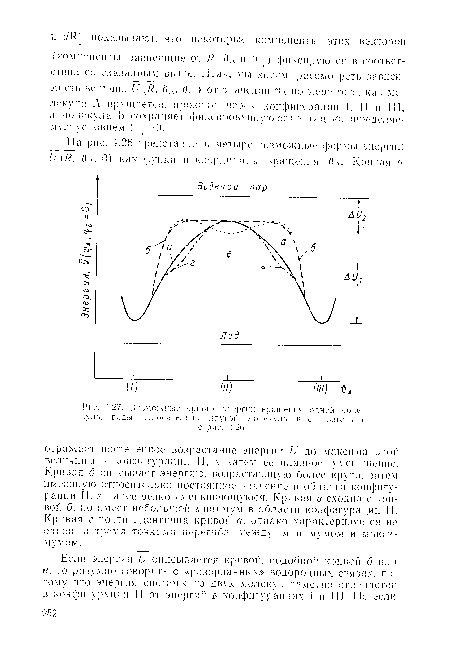
| Возможные кривые энергии вргпнения одной молекулы воды относительно другой молекулы в соответствии с рис. 4 ‘¿б. |
 |
Далее
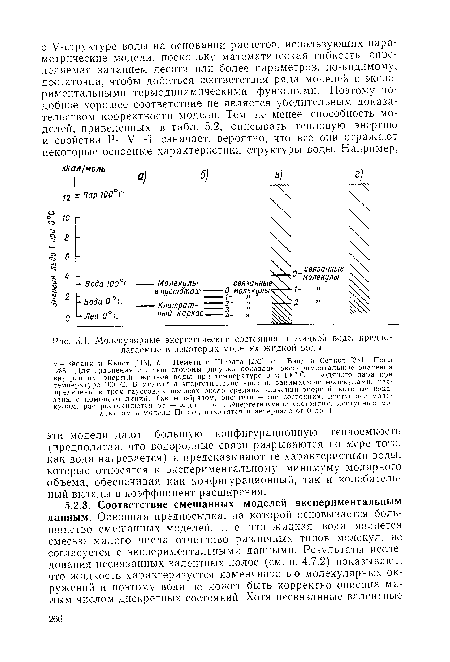
| Молекулярные энергетические состояния в жидкой воде, предполагаемые в некоторых моделях жидкой воды. |
 |
Далее
![Нормальные моды колебания Н20 [239].](/static/pngsmall/318624928.png)