Гидратация и зависящая от нее сила фонон-фононного взаимодействия (Ефф =£(Ус,е!!), где Ус(е!!) - объем (диэлектрическая проницаемость материала кластера)) резко промотируется при увеличении диэлектрической проницаемости (е!!), имеющем место вблизи точек фазовых переходов различного рода, увеличении заряда поверхности частицы, а также при уменьшении прочности поверхностной пленки (отделяющей сольватную и свободную воду) в результате адсорбции поверхностно-активных (ПАВ) веществ. Электромагнитные и магнитные поля также изменяют параметры сольватации, приводя к увеличению 2с1-слоев. Магнитная активация промотируется как прыжковой проводимостью зарядов, так и переходами, связанными с изменением спина в молекуле воды [34].[ ...]
Согласно формулировке, предложенной Крестовым [1751, под гидратацией ионов и молекул в общем случае понимается совокупность изменений, связанных с образованием ионного (молекулярного) раствора в воде. При гидратации происходит нейтрализация и перераспределение заряда ионов по окружающим их молекулам воды.[ ...]
Гидратация с последующей диссоциацией или образование в водной фазе новых продуктов сильно сказываются на динамике переноса молекул из газовой фазы в водно-капельную. Для описания этого процесса используется так называемая двухпленочная модель. В ней предполагается, что молекула при таком переходе преодолевает сопротивление пограничного слоя газовой и пограничного слоя жидкой фазы, расположенных по обе стороны границы раздела ’’воздух - вода".[ ...]
| Гидратация ионов в растворе (а), энтропия молекул воды в ближайшем окружении ионов (б) и коэффициент вязкости в уравнении Джонсона—Дола (в). | 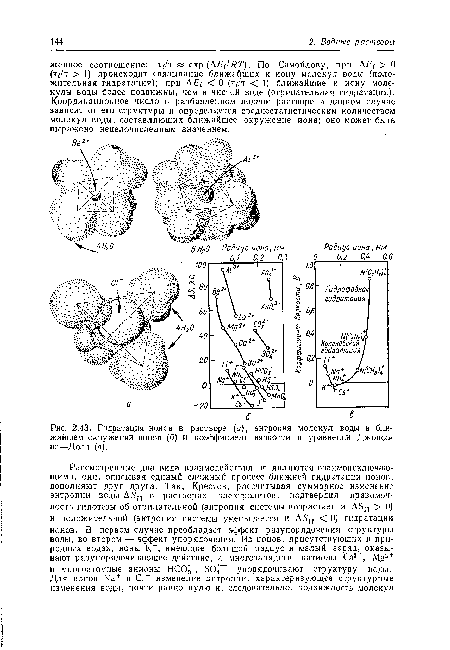 |
Влияние гидратации на устойчивость коллоидов изучено недостаточно, однако ясно, что оно неодинаково для золей гидрофильных и гидрофобных. Некоторая гидратация последних объясняется гидратацией адсорбированных ионов или молекул. После снижения заряда гидратные оболочки уже не препятствуют слипанию частиц. Коллоиды с гидрофильной поверхностью сохраняют устойчивость и после устранения заряда. Следовательно, наличие гидратных оболочек является для них более важным фактором стабилизации, чем двойной электрический слой [26].[ ...]
Если процесс гидратации осуществляется вслед за прокаливанием при достаточно низких температурах образца, то в той же области появляется широкая полоса 3680—3660 см 1, которая при тщательном изучении в действительности состоит из двух компонент: полос с частотами 3665 и 3450 см К По мнению Сидорова [41, 319], они характеризуют колебание адсорбированной воды.[ ...]
Вопрос о ближней и дальней гидратации ионов Крестов рассматривает с позиций преимущественного взаимодействия ион — молекулы воды и влияния возникающего комплекса на связи между самими молекулами воды. При оценке первого взаимодействия, названного термодинамической гидратацией, решающее значение имеет первичная гидратация ионов, определяющая структуру образующихся гидратов и вносящая наибольший вклад в энергетику процесса. Кроме координационных чисел, которые в данном случае имеют целочисленное значение, важнейшими количественными характеристиками процесса гидратации являются изменения термодинамических величин — энтальпии, энтропии, теплоемкости и изобарноизотермического потенциала.[ ...]
Характерно, что Л£> дальней гидратации для всех без исключения ионов — величина отрицательная, т. е. в этой области происходит уменьшение энтропии молекул воды и, следовательно, наблюдается только положительная гидратация —эффекты упорядочения здесь преобладают над эффектами разупорядочения. На абсолютное значение Д5дальн наиболее существенное влияние оказывает заряд ионов и меньше — их размер, соответственно изменяются и числа молекул воды в области дальней гидратации. При использовании термохимического метода для водных растворов электролитов типа I—I установлено, что количества молекул воды в I и II областях дальней гидратации для стехиометрических смесей ионов равны 30 и 60; дериватографическим методом в первой области дальней гидратации определены числа молекул для одно-, двух- и трехзарядных катионов, они оказались равными 30, 60 и 90.[ ...]
Влияние ионов на структуру воды связано с их гидратацией. Различают блнжнюю гидратацию (взаимодействие иона с ближайшими к нему молекулами воды) и дальнюю гидратацию — поляризацию более отдаленных молекул воды. Основной вклад в теорию гидратации ионов сделан О. Я. Самойловым, развившим молекулярно-кинетическое представление о гидратации ионов [6]. Характеристикой ближней гидратации является отношение времени пребывания молекулы воды в ближайшем окружении иона ко времени нахождения ее в положении равновесия с другими молекулами в невозмущенной структуре воды. На основании данных о растворимости солей и теплотах гидратации ионов установлено, что на связь одной молекулы с катионом в зависимости от его заряда ( + 1, +2 или +3) приходится соответственно 42, 126 или 420 кДж/моль. В последнем случае гидратированный катион похож на химическое соединение. Вблизи одновалентных ионов время оседлого пребывания молекул воды имеет порядок 10 8 с.[ ...]
Используя эти зависимости, Хорн показал, что наряду с кулоновской гидратацией ионов существует и гидрофобная гидратация молекул неполярных или гидрофобных веществ, а также присутствующих в растворе молекул газов. Сущность ее основана на окружении этих молекул клеткоподобной или клат-ратной гидратационной атмосферой.[ ...]
При добавлении к водным растворам флокулянтов веществ, способных к гидратации (неорганические соли — оксалаты, сульфаты или органические растворители — спирты, ацетон), растворимость флокулянтов уменьшается и они выделяются из раствора в твердом состоянии. Этот процесс называется высаливанием. Для высаливания необходимо брать такое количество реагентов, при котором образуются близкие к насыщейию растворы солей или смеси, содержащие >60% органических растворителей.[ ...]
| Схема электрострикции в водном растворе (а) и трехзонная модель гидратации ионов (б). | 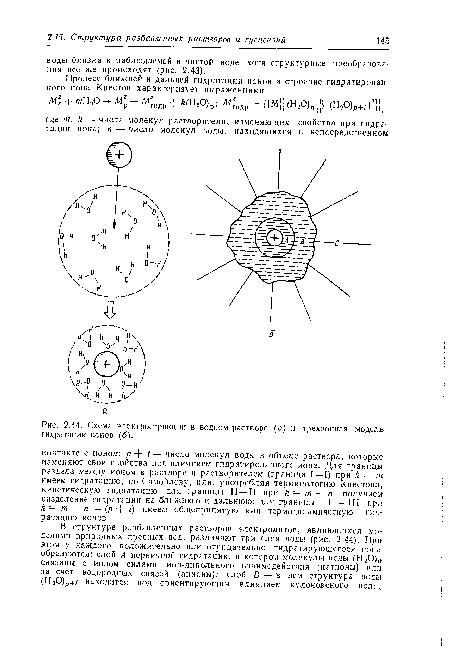 |
Изофермент С является чрезвычайно эффективным катализатором. Для реакции гидратации Исах равна 106с-1, а /См для СОг — 8,3 мМ, в то время как для реакции дегидратации са4 = 6-105 с-1, а /См для НСОз равна 32 мМ [215]. Каталитическая активность фермента определяется состоянием ионизации группы с р/Са = 7 в свободном ферменте [215]. Реакция гидратации зависит от доли этих групп, находящихся в основной форме, а реакция дегидратации — от доли этих же групп, находящихся в кислой форме. Число оборотов для указанных реакций Значительно выше констант скорости переноса протонов между водой и группой с р/Са = 7 (приблизительно 2-103 с-1; табл. 4.2). В нефизиологических реакциях эти ферменты катализируют также гидратацию альдегидов и гидролиз эфиров.[ ...]
Экспериментальным подтверждением резонансного характера (стимулирования) гидратации вблизи точек фазовых переходов, а также дистантного взаимодействия ассоциатов вследствие их фонон-фононного взаимодействия, могут являться результаты, полученные авторами работы [48] с использованием хемилюминесцентного метода анализа радикалов в воде, а также ранее полученные результаты исследований возбуждения, поляризации и распада электрохимически активированных водных аэрозолей в полях электромагнитных волн [34,48].[ ...]
Вызывает интерес тот факт, что при взаимодействии анйона с водой происходит гидратация протона аниона с образованием «она гидроксония НзО+. О наличии ©го можно судить по имеющемуся в спектрах кислых солей поглощению в области 2700—3100 и — 1750 см-• и слабому поглощению при 2100 и 2200 см х [140].[ ...]
Изоборнеол в природе в свободном состоянии не существует и его получают при гидратации камфена (через изоборниловые эфиры).[ ...]
Вещества, образующиеся при взаимодействии основных окислов с водою, т. е. при гидратации основных окислов, носят название оснований. Водные растворы оснований называются щелочами. При взаимодействии кислотных окислов с водою образуются кислоты.[ ...]
Коллоиды почвы обладают способностью поглощать молекулы воды. Эта способность называется гидратацией коллоида. Гидрофобные коллоиды практически не гидратируются, почвы характеризуются плохой смачиваемостью, при насыщении почвы высоко-гидратированными катионами происходит пептизация почвенных коллоидов.[ ...]
Адсорбция ухудшается при накоплении в молекулах гидроксильных групп, обладающих большой энергией гидратации за счет водородных связей. Наличие электрического заряда, ориентирующего вокруг себя диполи воды, также ухудшает адсорбцию. В связи с этим диссоциированные на ионы молекулы сорбируются значительно меньше, чем недиссоциированные молекулы тех же веществ.[ ...]
Отсюда понятно, что при выработке подобных видов бумаги целесообразно исключить факторы, вызывающие гидратацию волокон, и в первую очередь воду — основной фактор гидратации. Сказанное является предпосылкой для применения при выработке пористых видов бумаги размола волокон в воздушной среде.[ ...]
Все изменения структуры воды, вызываемые появлением в ней иона, принято делить на «ближнюю» и «дальнюю» гидратацию. Под первой понимается взаимодействие иона с ближайшими к нему молекулами воды. Дальняя гидратация заключается в поляризации под действием поля ионов молекул воды, не входящих в его ближайшее окружение. Обобщая и анализируя большой экспериментальный материал, О. Я. Самойлов ввел понятие положительной и отрицательной гидратации ионов. В первом случае ионы довольно устойчиво связаны с ближайшими к ним молекулами воды. При отрицательной гидратации молекулы воды вблизи ионов становятся более подвижными, чем в чистой воде. Это сложное явление обычно анализируется при условном делении гидратной оболочки на два слоя.[ ...]
Известно, что в процессе твердения цементного камня одновременно протекает ряд сложных процессов: растворение и гидратация цементных минералов с образованием пересыщенных растворов, самопроизвольное диспергирование этих минералов до частиц коллоидных размеров, образование тиксотропных коагуляционных структур и, наконец, возникновение, рост и упрочнение кристаллизационных структур. Следовательно, влияние магнитной обработки воды, используемой для растворения, на твердение и свойства цементного камня является вполне закономерным.[ ...]
Рассмотренные два вида взаимодействия не являются взаимоисключающими, они, описывая единый сложный процесс ближней гидратации ионов, дополняют друг друга. Так, Крестов, рассчитывая суммарное изменение энтропии воды Д5П в растворах электролитов, подтвердил правомочность гипотезы об отрицательной (энтропия системы возрастает и ДБ > 0) и положительной (энтропия системы уменьшается и Д5П < 0) гидратации ионов. В первом случае преобладает эффект разупорядочения структуры воды, во втором — эффект упорядочения. Из ионов, присутствующих в природных водах, ионы К+, имеющие большой радиус и малый заряд, оказывают разупорядочивающее действие, а многозарядные катионы Са2+, Д 2 + и многоатомные анионы НСО ", упорядочивают структуру воды.[ ...]
Для дальнейшего усовершенствования способов получения терпингидрата на Московском терпинеоловом заводе для реакции гидратации был применен другой, более активный катализатор — смесь серной кислоты и пара-толуолсульфокислоты.[ ...]
| Зависимость количества фиксированного , аОН для нативной (/) и мерсеризованной (II) целлюлозы и его средней степени гидратации (III) от концентрации раствора едкого натра. | 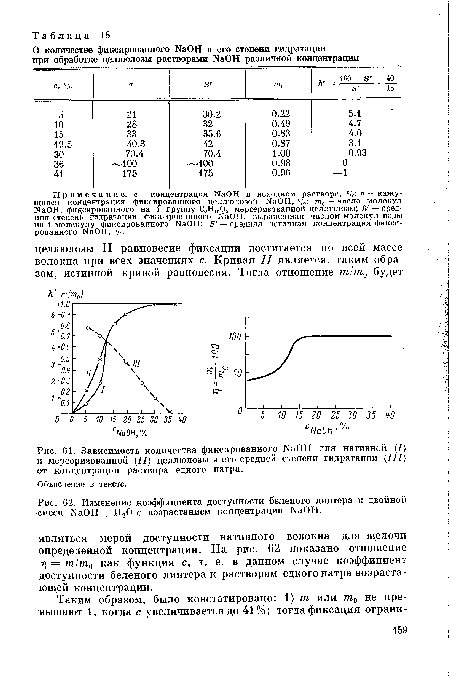 |
Существенный недостаток сернокислого алюминия — его чувствительность к температуре очищаемой воды, что объясняется большой гидратацией гидроокиси алюминия при низких температурах. Возрастание гидратации при низких температурах (—1—2° С) способствует стабилизации золя гидроокиси алюминия, плохо коагулируемого в этом случае ионами НС03 и SO - даже в концентрациях, в несколько раз превышающих их обычное содержание в воде. Повышение устойчивости золя сильно влияет на скорость хлопьеобразования. Этим и объясняется то, что при использовании сернокислого алюминия в условиях низких температур наблюдается замедление процесса хлопьеобразования, попадание остаточного алюминия в очищенную воду и осаждение гидроокиси алюминия в трубах.[ ...]
Водные молекулы прочно связаны с ионами растворенного вещества и участвуют с ними как одно целое в броуновском движении. Второй вид гидратации объясняется взаимодействием ионов с молекулами воды, не входящими в ближайшее окружение. Молекулы воды испытывают лишь незначительное влияние ионных полей без потери поступательных степеней свободы. Толщина «ближнего» гидратного слоя имеет молекулярные размеры, а число молекул воды, удерживаемых ионами в этом слое, называется координационным числом (или лигандностъю) и является важной количественной характеристикой гидратации. Лиганд-ность ионов зависит от их природы, концентрации электролита, температуры и некоторых других условий.[ ...]
Технология включает в себя следующие процессы: охлаждение газа до заданной температуры в реакторе, конверсию S02 в S03 на поверхности катализатора, гидратацию S03 в H2S04 и конденсацию паров H2S04 в конденсаторе WSA.[ ...]
Накагава и Курияма [5] предложили теорию ассоциации молекул неионогенных ПАВ, в которой основным фактором, препятствующим ассоциации молекул, является теплота гидратации полярных групп и конформационные изменения энтропии гибкой гидрофильной цепи молекулы ПАВ.[ ...]
Традиционное объяснение состоит в том, что подвижность ионов связывают с их радиусом. Так как радиус иона лития наименьший, то ион должен иметь наибольшее число гидратации п, поэтому, вероятно, подвижность столь сильно гидратированного иона становится малой. Значит, и электрическая проводимость иона лития — наименьшая в данном ряду. Радиус иона натрия несколько больше, число гидратации для него немного меньше, а в результате и электрическая проводимость чуть выше. Рассуждая подобным образом, можно прийти к выводу о непрерывном возрастании электрической проводимости в данном ряду растворов солей, что, однако, противоречит опыту. Поэтому традиционное объяснение постулирует одинаковость числа п для ионов калия, рубидия и цезия. Но это противоречит данным о числах гидратации, полученных другими методами. Так, из результатов измерений скорости звука получаются следующие значения п: и+ — 4, Ь1а+ — 6, К+ — 5, ИЬ+ — 3, Св+ —2[ ...]
Увлажнение крупного заполнителя почти не увеличивает его объем. Однако некоторые виды щебня поглощают до 2% воды. Чтобы не уменьшился объем воды, необходимой для гидратации цемента, незадолго перед смешиванием составных частей бетона щебень в куче надо полностью насытить влагой, но к моменту загрузки щебня в бетономешалку его поверхность должна высохнуть. Щебень дозируют так же, как и песок. Нельзя насыпать щебень в дозировочный ящик выше уровня стенок ящика. Щебень разного гранулометрического состава надо держать в отдельных кучах и брать для смеси необходимое количество щебня из каждой кучи.[ ...]
Перспективным способом получения гипсовых изделий является совмещение процессов формования их из дигидрата, дегидратации в герметичной форме при нагревании и последующей гидратации водой, выделившейся при охлаждении в капельножидком состоянии /72/. Дегидратация фосфогипса в крепких солевых растворах при температуре выше 100 °С в принципе обеспечивает высокую прочность вяжущего,но требует тщательной отмывки готового продукта от солей горячей водой. Неизбежность последующей упарки больших количеств промывных вод существенно повышает стоимость производства.[ ...]
При размоле растительных волокон в водной среде происходит как чисто механический процесс изменения размеров и формы волокон, так и коллоидно-химический процесс, называемый гидратацией волокон. Явления механического характера выражаются в укорачивании волокон и их продольном расщеплении на фибриллы. В данном случае под термином гидратация понимаются не образование гидратов, а коллоиднохимические явления, начинающиеся с набухания гидрофильных растительных волокон и, как будет показано ниже, придающие волокнам способность связываться между собой с образованием прочной структуры листа.[ ...]
Начиная с архея, масса свободной воды на Земле была сравнительно мала, что позволяет достаточно условно называть имевшиеся тогда моря «мировым океаном». Породы земной коры подвергались гидратации и углекислый газ весьма слабо связывался в карбонатах, что обусловило повышенное парциальное атмосферное давление.[ ...]
Нам представляется, что значительную роль могут играть большие ускорения движения ионов в начальный момент вхождения в магнитное поле, особенно высокоградиентное. При таком ускорении дальняя гидратация ионов может на какое-то мгновение уменьшиться, что также способствует взаимодействию противоионов.[ ...]
Производство фосфорной кислоты при огневой переработке фосфорных шламов, как и при использовании для этой цели элементного фосфора, состоит из следующих стадий: сжигание шлама; охлаждение газов; гидратация и абсорбция фосфорного ангидрида; конденсация фосфорной кислоты; улавливание туманообразной фосфорной кислоты. Все стадии технологического процесса, за исключением улавливания туманообразной кислоты, могут осуществляться в одном аппарате. В промышленности применяют много различных технологических схем установок, состоящих, как правило, из двух или трех основных аппаоатов [269].[ ...]
Защищенные частицы золей имеют примерно ту же величину ДП, что и макромолекулы ВМВ. По современным представлениям коллоидная защита является следствием возникновения или усиления разных факторов стабилизации: гидратации поверхности частиц [13 (стр. 305), 39, 40], увеличения - -потенциала частиц [13 (стр. 305), 41], взаимного отталкивания гибких макромолекул, адсорбированных на частицах золя [42]. Адсорбция защитного вещества на поверхности частиц продуктов гидролиза многовалентных металлов может сопровождаться химическим взаимодействием с образованием в поверхностных слоях гидрофильных комплексов [43, 44].[ ...]
Значительным недостатком всех приведенных теорий является отсутствие в них указаний на роль в процессе конденсационного образования твердой фазы среды, в которой происходит осаждение и влияние ее на структуру осадка. Особенно важна роль гидратации при выделении осадков гидроокисей алюминия и железа. Последние, как известно, оседают в очень гидратированном виде и в отдельных случаях дают даже студни. Объяснить эти явления можно лишь сильной гилрофйльностью частиц гидроокисей.[ ...]
Вначале изучалась экстракция Fe(III) и Т1(Ш) из хлоридных растворов. Эти системы интересовали нас главным образом как типовые модельные системы. Можно считать, что механизм экстракции образующихся при этом соединений, особенно в его части, касающейся гидратации и сольватации, является в значительной мере общим для соединений такого типа.[ ...]
Адсорбция растворенных веществ является результатом перехода молекул растворенного вещества из объема раствора на поверхность твердого сорбента под действием силового поля поверхности. При этом конкурируют два вида межмолекулярного взаимодействия: гидратация молекул растворенного вещества, т. е. взаимодействие их с молекулами воды в растворе, и взаимодействие молекул адсорбирующегося вещества с атомами поверхности твердого тела. Разность энергий этих двух процессов и есть та энергия, с которой извлеченное из раствора вещество удерживается на поверхности погруженного в раствор адсорбента. Чем больше энергия гидратации молекул растворенного вещества, тем большее противодействие испытывают эти молекулы при переходе на поверхность адсорбента и тем слабее вещество адсорбируется из водного раствора.[ ...]
Близкой к описанной выше является технология гранулирования фосфогипса, предложенная фирмой «Опоёа» (Япония). На первой стадии процесса осуществляют дегидратацию фосфогипса—до образования фосфополугидрата или растворимого ангидрита. Затем проводят гидратацию обезвоженного продукта в присутствии известкового молока. При этом на стадии дегидратации фосфогипса происходит вытеснение Р205(вод.), а затем образование нерастворимого фосфата. Растворимые соединения фтора после нейтрализации известковым молоком также переходят в нерастворимые фториды. В процессе гидратации фосфополугидрата известковым молоком происходит гранулирование фосфогипса с получением гранул, прочность которых отвечает требованиям при транспортировании и хранении. Размеры получаемых гранул 5—20 мм при общей влажности 10—15 %.[ ...]
Основную роль в процессе флотации диспергированных примесей играют поверхностные силы [2], ван-дер-ваальсовские силы притяжения, электрические силы, возникающие при перекрытии двойных электрических слоев, образующихся вокруг частички в водном растворе, и силы гидратации любых гидрофильных групп на поверхности частички. Действия этих трех сил определяют смачиваемость, или несмачиваемость частицы водой. Прилипание частицы к газовому пузырьку тем сильнее, чем хуже ее смачивание водой. Мерой смачиваемости твердого ?ела жидкостью является краевой угол смачивания, измеряемый обычно со стороны воды (рис. Ш-2). Полное смачивание водой будет при 0 = 0° и полное прилипание к воздуху (т. е. не-смачивание водой) при 0 = 180°. Однако вещества, краевой угол смачивания водой которых превышал бы 150° (у твердого парафина), неизвестны; количество же веществ, у которых 0 = 0°, очень велико.[ ...]
Оказалось, что в этом случае снижается отрицательная адсорбция ионов железа на поверхности раздела раствор — воздух. По-видимому, рассматриваемое явление связано со значительным уменьшением гидратации катиона железа [157]. Таким образом, временное изменение магнитной обработкой дальней гидратации ионов в водных системах может явиться одним из существенных механизмов регулирования физико-химических свойств последних.[ ...]
Наряду с перечисленными направлениями утилизации дистиллерных шламов содовых производств перспективным считают их использование (через бесцементное вяжущее) для замены цемента при приготовлении тампонажных материалов, для производства асфальтобетонов (в качестве активизатора гидратации и наполнителя) и по некоторым другим технологически» направлениям.[ ...]
Особого типа взаимодействия наблюдаются при появлении в таком структурированном растворителе, как вода, соединений, диссоциирующих на ионы, когда сочетаются чисто физические явления, обусловленные присутствующими в стехиометрических соотношениях положительными и отрицательно заряженными частицами, с явлениями нарушения структурных элементов среды, характеризуемых общим термином «гидратация ионов». Физико-химические свойства таких систем и соответствующих им по составу природных вод будут различны в зависимости от наличия в них однозарядных (йа+ и К+) или двухзарядньпс (Са2+ и Л 2+) катионов, а также одноатомных (С1—) или многоатомных (НСОэ и Б01 ) анионов. Важность высказанного положения становится ясной, если напомнить, что при исследованиях химических процессов водоподготовки еще недостаточно внимания уделяется изучению влияния ионных примесей воды на кинетику этих процессов. Эю затрудняет статистическую обработку накопленных обширных материалов по эксплуатации станций подготовки воды с различной минерализацией.[ ...]
Обычно для суждения о структурном состоянии воды и ее растворов используют результаты измерения вязкости. Почти все электролиты, которые встречаются в природных водах, увеличивают вязкость воды, и среди них особенно выделяются сульфат магния, а также добавляемые в воду коагулянты — сульфат алюминия и хлорид железа (III). Однако хлорид калия фактически делает воду менее вязкой. Все это удовлетворительно объясняется описанной выше положительной и отрицательной гидратацией ионов, входящих в состав электролитов, в связи с чем первые называются структуроупорядочивающими, последние — структуроразрушающими электролитами (рис. 2.45, 2.46).[ ...]
Необходимость определения примесей в этаноле обусловлена контрабандой некачественного спирта и фальсификацией водки и других алкогольных напитков. Такие анализы обычно проводят методом газовой хроматографии (см. главу I), которая является лучшим методом для обнаружения примесей метанола, альдегидов и сивушных масел как в самом этаноле, так и в алкогольных напитках. Однако современные технологии позволяют получать очень «чистый» спирт, с минимальным содержанием примесей. В таком случае бывает практически невозможно (методом газовой хроматографии) отличить этанол, полученный из пищевого сырья (зерно, картофель, свекла и др.), от синтетического этилового спирта (получается гидратацией этилена) или гидролизного (получают гидролизом древесины).[ ...]
При растворении электролитов в воде наблюдается явление электро-стрикции — кулоновские поля образующихся в растворе ионов взаимодействуют с диполями молекул воды достаточно сильно, вследствие чего вблизи ионов происходит сжатие растворителя, это подтверждается измерениями скорости ультразвука в таких водных системах. Структура воды при этом заметно искажается находящимися в ней ионами: ионы небольшого размера помещаются в пустотах надмолекулярных образований, ионы средних размеров (например, одновалентные ионы щелочных металлов и ионы двухвалентного бериллия) имеют координационное число, равное четырем, и, очевидно, замещают молекулы воды в структурных узлах. Гидратированные ионы двухвалентных кальция и магния и трехвалентного алюминия могут быть представлены в виде октаэдров, в центре которых находятся ионы этих металлов, электростатически связанные с шестью молекулами воды, расположенными в их вершинах. Эти шесть молекул воды и составляют первую координационную сферу гидратированных многозарядных катионов. Отмеченное ион-дипольное взаимодействие наиболее характерно для гидратации катионов, при гидратации анионов со значительным зарядом или малым радиусом типично присоединение молекул воды за счет водородных связей.[ ...]