При исследовании электрохимических реакций и выявлении механизма процессов, как уже было показано (см. п. 3.3.1), существенную роль играют процессы переноса вещества к поверхности электрода, т. е. массоперенос.[ ...]
Перенос вещества из глубины раствора к поверхности электрода осуществляется несколькими путями, наиболее важным из которых является молекулярная диффузия. Другим способом доставки реагирующих частиц является перенос под действием электрического поля, называемый миграцией, которая наблюдается только для заряженных частиц. Наконец, третьим путем доставки вещества к поверхности электрода является конвекция, т. е. перенос вещества вместе с потоком движущейся жидкости.[ ...]
Молекулярная диффузия и предельный ток. В равновесных условиях концентрация вещества, во всех точках раствора за пределами ДЭС одинакова. При пропускании тока вблизи электрода происходит нарушение равновесия (за счет расходования вещества в электродной реакции) и возникает разница в концентрации частиц у поверхности электрода и в объеме раствора, что и приводит к диффузии вещества из глубины раствора к наружной границе ДЭС, а продуктов реакции — в глубь раствора.[ ...]
Уравнение (3.58) выражает скорость электродного процесса при замедленной диффузии, причем оно справедливо при избытке фонового электролита, т. е. когда миграцией практически можно пренебречь. Это уравнение удобно представить в виде графика (рис. 3.11).[ ...]
При больших отрицательных Т1Д экспонентой можно пренебречь по сравнению с единицей и гд=гдпР.[ ...]
Миграция частиц под действием электрического поля. Как уже указывалось, ток, обусловливающий перенос заряженных частиц, называется миграционным током (1М). При электроокислении миграция способствует подходу анионов и замедляет подход катионов. В случае электровосстановления наблюдается обратная картина.[ ...]
Конвективный перенос вещества. Предельное значение тока, создаваемого диффузией и миграцией, относительно невелико вследствие малых скоростей потоков. Чтобы повысить эту величину, необходимо проводить перемешивание раствора, т. е. увеличивать перенос вещества совместно с потоком движущейся жидкости, называемый конвективным переносом, однако перемешивание может возникнуть и в естественных условиях. Так, изменение концентрации приводит к изменению плотности раствора и возникновению потоков жидкости. Изменение плотности может вызвать также выделение газа на электродах и разогрев электролита.[ ...]
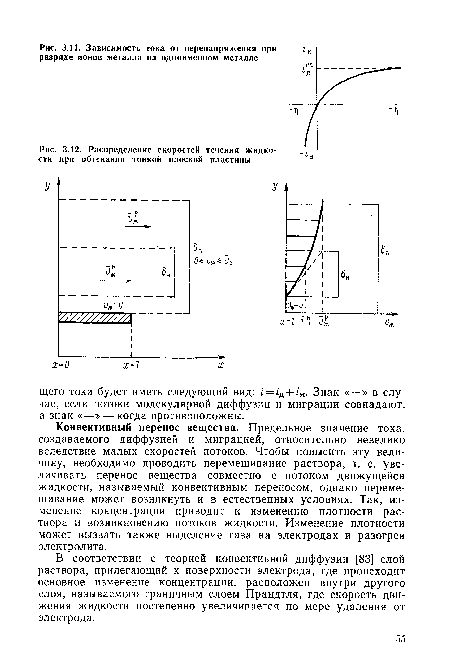
В соответствии с теорией конвективной диффузии [83] слой раствора, прилегающий к поверхности электрода, где происходит основное изменение концентрации, расположен внутри другого слоя, называемого граничным слоем Прандтля, где скорость движения жидкости постепенно увеличивается по мере удаления от электрода.[ ...]
В слое Прандтля следует выделить толщину слоя Нернста 6ц, в котором концентрация диффундируемого вещества понижается от значения С0 в глубине раствора до значения С6 , которое характерно для раствора непосредственно около границы фаз, где устанавливается стационарный градиент концентрации, характерный для диффузии в неперемешиваемом ограниченном объеме. Толщина слоя Прандтля в ламинарном режиме [83].[ ...]
Если скорость процесса контролируется кинетикой, то ток не зависит от подвода вещества и от скорости вращения диска. С помощью измерений на вращающемся дисковом электроде можно по предельному току вычислить коэффициенты диффузии отдельных ионов или молекул. При известном коэффициенте диффузии (вычисленном, например, из подвижностей) можно по величине ¿дРопределить число электронов (г), участвующих в электродном процессе. Это имеет практическую ценность при установлении механизма реакций, протекающих с участием органических веществ.[ ...]
Рисунки к данной главе:
| Распределение скоростей течения жидкости при обтекании тонкой плоской пластины |
 |