Величина, обратная сопротивлению (1/Яэ), называется электрической проводимостью и выражается в сименсах (См).[ ...]
Теоретически чистая вода имеет электропроводность 0,038 10 6, талая (дождевая) вода—(1 -ь5) • 10-5, природная вода средней минерализации (200- -500 мг/л) — (5-М0) • 10-5, сточная вода — ю -ио-1 Ом-1-см-1.[ ...]
Величина хд различных растворов электролитов зависит от их ионного состава и концентрации. Зависимость хд = /(С) характеризуется максимумом, что объясняется увеличением межионного взаимодействия в электролите при повышении его концентрации. Для большинства электролитов такой максимум наблюдается при концентрациях 100—200 г/л, что не характерно для природных и сточных вод. Для слабоконцентрированных солей (0,5—5 г/л) может быть принят линейный характер зависимости электропроводности от концентрации.[ ...]
При оценке проводимости раствора используют также эквивалентную электропроводность, характеризующую электропроводность раствора, в объеме которого содержится 1 г-экв электролита.[ ...]
Эквивалентную электропроводность рассчитывают из экспериментально определяемых значений хд с учетом концентрации С раствора электролита. Если концентрация раствора выражена в молях, то эквивалентная электропроводность характеризуется как молярная и выражается в м2/Ом-моль.[ ...]
Так как рт<Сат, то зависимости носят практически линейный характер в широком интервале температур. Для сильных кислот ат 0,0164, для щелочей ат 0,0190, для солей ат»0,0220.[ ...]
Для среднего газосодержания в межэлектродном пространстве (Г = 0,014-0,04) влияние этой фазы на электропроводность незначительно и может не учитываться в практических расчетах. Однако при малых расстояниях между электродами (4<5 мм) Г может резко возрастать и это влияние окажется более заметным.[ ...]
А% и Вя — величины, зависящие от температуры, вязкости раствора и диэлектрической проницаемости среды. Для одно-двухза-рядного электролита при 25 °С Кя = 1,914- 10 4 + 7,258 10 3 Яо.[ ...]
Относительную подвижность ионов и,0 называют ионной эквивалентной электропроводностью и выражают в Ом-1 • м2 • г-экв.[ ...]
Определение электропроводности электролита производится с помощью мостов сопротивления, питаемых переменным током с частотой 500—1000 Гц.[ ...]
Рисунки к данной главе:
| Изменение в зависимости от концентрации катионов (а) и анионов (б) без учета Н+, К+, С! |
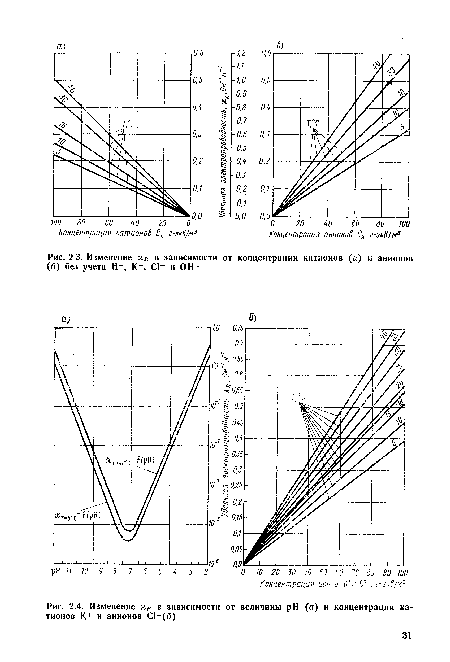 |
| Изменение в зависимости от величины pH (а) и концентрации катионов К+ и анионов С1_(б) |
 |
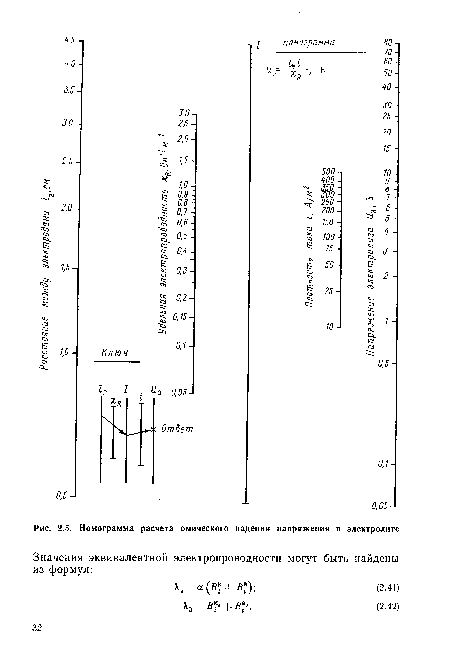
| Номограмма расчета омического падения напряжения в электролите |
 |