Процессы ионного обмена широко используются в технике подготовки воды для энергетических и технологических нужд. В последние годы увеличение производства ионообменных материалов и расширение их ассортимента сделало возможным более широкое применение их в технологии очистки промышленных сточных вод.[ ...]
Ионообменные материалы — твердые, нерастворимые в воде вещества, в структуру которых входят группы атомов, несущие электрический заряд, скомпенсированный подвижными ионами противоположного знака. Эти «противоионы» способны замещаться любыми другими ионами того же знака, находящимися в растворе, контактирующем с ионообменными материалами. В результате устанавливается ионообменное равновесие, смещающееся при изменении концентрации раствора, валентности противо-ионов в растворе, температуры и других факторов, подобно равновесию в растворе смеси двух солей, существенно отличающихся по растворимости.[ ...]
Проводя далее эту аналогию, можно представить катионообменный материал, как нерастворимую соль (Кат) Ме+ или кислоту (Кат) Н+, где (Кат)-—нерастворимый скелет вещества, обладающий отрицательным зарядом, а Ме+ или Н+ — противоионы, компенсирующие заряд нерастворимого скелета или, как часто говорят, «матрицы» ионита.[ ...]
Промышленные анионообменные материалы — преимущественно смолы, содержащие первичные, вторичные и третичные аминогруппы или четвертичные азотистые основания либо включающие в свою структуру азотистые гетероциклы.[ ...]
Анионообменные смолы, содержащие преимущественно первичные аминогруппы, являются слабоосновными и поглощают анионы только из растворов сильных электролитов. Смолы, содержащие третичные и четвертичные аминогруппы,— сильноосновные и хорошо поглощают ионы даже слабо диссоциированных электролитов.[ ...]
Обмен противоионов осуществляется в эквивалентных количествах, если при этом не протекают дополнительные процессы, приводящие к фиксации противоионов и искажающие основную картину ионного обмена. Обычно при обмене небольших неорганических ионов ионообменное равновесие устанавливается быстро и уже в течение первых секунд степень приближения к равновесию достигает 90—98%.[ ...]
При более детальном ознакомлении с процессом ионного обмена проявляются, однако, довольно существенные отличия его от реакций обмена между солями разной растворимости. Сетчатая структура синтетических ионов, способность их к набуханию и обусловленные этим изменения осмотического давления внутри ионита, изменение гидратации ионов в смоле, вызванное ограниченным размером ячеек ее сетчатой структуры, высокая концентрация фиксированных ионогенных групп и противоионов в ионите, создающая довольно сильное электростатическое поле в смоле, диффузионные затруднения при обмене крупных ионов — все это усложняет ионный обмен. Многие из указанных особенностей обмена ионов наиболее сильно проявляются при обменном поглощении крупных органических ионов, а именно такие ионы и существуют в водных растворах ПАВ. Вследствие этого использование ионообменных процессов для извлечения анионных и катионных ПАВ из сточных вод потребовало предварительного изучения поведения ПАВ при контакте с синтетическими ионообменными смолами различного строения.[ ...]
К физическим характеристикам ионообменных материалов относятся объемный вес в сухом и набухшем состоянии, объем пустот между зернами в единице объема зерен набухшего ионита и гранулометрический состав.[ ...]
Синтетические органические материалы могут весьма существенно отличаться густотой сетки, образованной углеводородными цепями полимерной молекулы. Эта пространственная сетка — результат введения соединений, образующих при синтезе поперечные мостики между длинными полимерными цепями. Одним из наиболее распространенных так называемых «сшивающих» компонентов полимерных ионообменных смол является ди-винилбензол. В зависимости от его процентного содержания (или, как говорят, «процента сшивания») ионообменные смолы могут больше или меньше набухать в воде, т. е. имеют различную сетчатую структуру. Естественно, что сильно «сшитые» смолы обладают меньшей доступностью для крупных ионов и избирательно поглощают ионы меньших размеров. Органические ионы такими смолами поглощаются мало [!]• Мало «сшитые» смолы при набухании сильно увеличиваются в объеме и в просветы между полимерными углеводородными цепями их сетчатой структуры (матрицы) крупные органические ионы диффундируют относительно легко [2].[ ...]
Согласно этому, Поль и сотрудники [3] обнаружили, что ионы алкиларилсульфоната (анионное ПАВ — дюбарал) поглощались анионообменными смолами в тем меньших количествах, чем больше сшивающего компонента (дивинилбензола) вводили в ионит при его синтезе.[ ...]
Рисунки к данной главе:
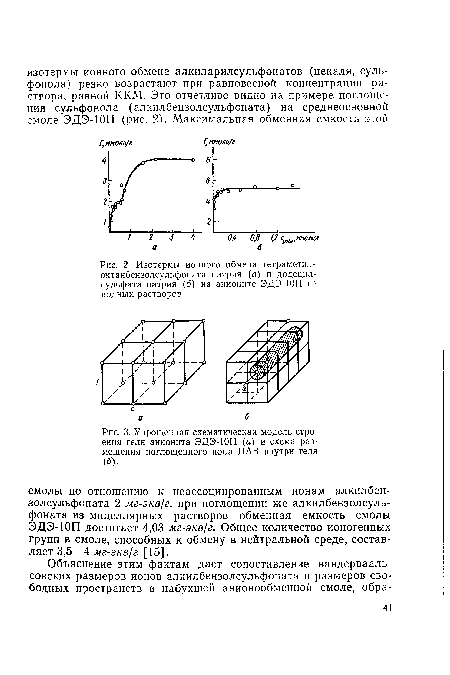
| Упрощенная схематическая модель строения геля анионита ЭДЭ-10П (а) и схема размещения поглощенного иона ПАВ внутри геля (б). |
 |