Полярографический метод анализа основан на измерении предельного тока диффузии, возникающего при электролизе раствора с помощью ртутных или других электродов.[ ...]
Исследуемый раствор подвергают электролизу при непрерывно изменяющемся напряжении. При наличии в растворе ионов, способных восстанавливаться или окисляться при определенном потенциале, в момент их разряжения на электроде возникает соответствующая сила тока. Для измерения силы тока в электрическую систему включают зеркальный гальванометр.[ ...]
При применении ртутных электродов катодом служат капли ртути, вытекающие с определенной скоростью из капилляра, анодом — слой ртути, имеющий по сравнению с катодом гораздо большую поверхность. Источником тока служит аккумуляторная батарея на 4—6 в (батареи кислотные или щелочные). Ток от аккумулятора подается на потенциометр с подвижным контактом, позволяющим подводить к электролизеру напряжение от 0 до 4 в. Для этой цели удобно пользоваться барабанным мостиком, представляющим собой равномерно намотанную на барабан константановую проволоку общим сопротивлением 15—16 ом.[ ...]
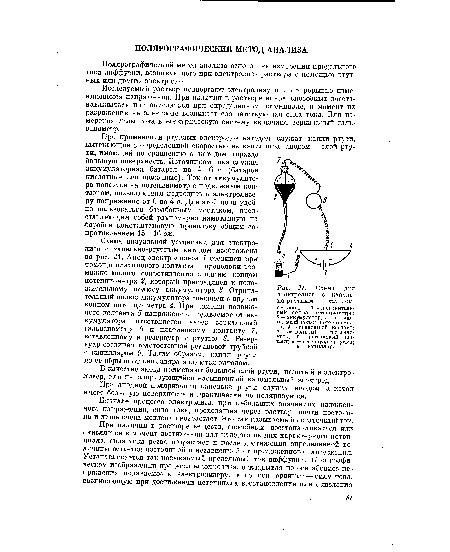
Схема визуальной установки для электролиза с капельно-ртутным катодом изображена иа рис. 21. Анод электролизера 1 соединен при помощи платинового контакта и проволоки возможно малого сопротивления с одним концом потенциометра 2, который присоединен к положительному полюсу аккумулятора 3. Отрицательный полюс аккумулятора соединен с другим концом потенциометра 4. При помощи подвижного контакта 5 напряжение, подаваемое от аккумулятора, ответвляется через зеркальный гальванометр 6 к платиновому контакту 7, вставленному в резервуар с ртутью 8. Резервуар соединен толстостенной резиновой трубкой с капилляром 9. Таким образом, капли ртути до ее обрыва от капилляра являются катодом.[ ...]
В качестве анода применяют большой слой ртути, налитый в электролизер, или неполяризующийся насыщенный каломельный электрод.[ ...]
При анодной поляризации капельки ртути служат анодом, а катод имеет большую поверхность и практически не поляризуется.[ ...]
Вначале процесса электролиза, при небольших значениях наложенного напряжения, сила тока, проходящая через раствор, почти постоянна и лишь очень медленно возрастает. Это так называемый остаточный ток.[ ...]
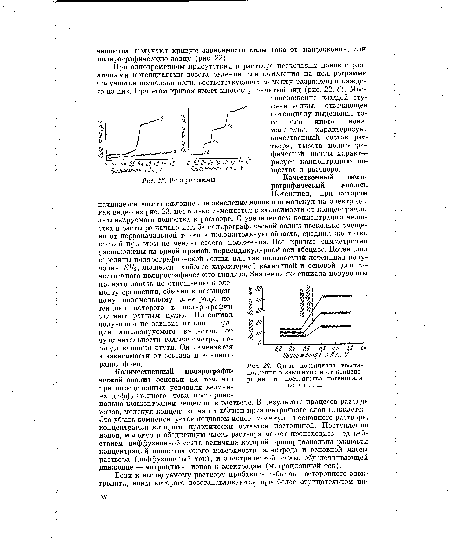
При одновременном присутствии в растворе нескольких ионов с различными потенциалами восстановления или окисления на полярограмме получается несколько волн, соответствующих моменту разряжения каждого из них. При этом кривая имеет многоступенчатый вид (рис. 22, б). Местоположение каждой ступени волны, отвечающее потенциалу выделения того или иного иона, молекулы, характеризует качественный состав раствора; высота полярографической волны характеризует концентрацию вещества в растворе.[ ...]
Качественный полярографический анализ. Потенциал, при котором начинается восстановление или окисление ионов или молекул на электроде, как видно из рис. 23, несколько изменяется в зависимости от концентрации анализируемого вещества в растворе. С увеличением концентрации вещества в растворе начало изгиба полярографической волны несколько смещено от первоначальной точки в положительную область, средняя же точка кривой при этом не меняет своего положения. Все кривые симметрично расположены на одной прямой, перпендикулярной оси абсцисс. Потенциал середины полярографической волны, или так называемый потенциал полуволны Е11ъ, является наиболее характерной величиной и основой для качественного полярографического анализа. Значение потенциала полуволны принято давать по отношению к элементу сравнения, обычно к насыщенному каломельному электроду, потенциал которого в полярографии считают равным нулю. Потенциал полуволны не зависит от концентрации анализируемого вещества, от чувствительности гальванометра, периода капания ртути. Он изменяется в зависимости от состава и концентрации фона.[ ...]
Количественный полярографический анализ основан на том, что при определенных условиях величина диффузионного тока пропорциональна концентрации вещества в растворе. В результате процесса разряда ионов, молекул концентрация их вблизи приэлектродного слоя снижается. Эта убыль компенсируется подводом ионов, молекул из основного раствора, концентрация которого практически остается постоянной. Поступление ионов, молекул в обедненную часть раствора может происходить под дехг-ствием диффузионной силы, величина которой пропорциональна разности концентраций вещества около поверхности электрода и основной массы раствора (диффузионный ток), и электрической силы, обусловливающей движение — миграцию — ионов к электродам (миграционный ток).[ ...]
Рисунки к данной главе:
| Сдвиг потенциала восстановления в зависимости от концентрации и постоянства потенциала полуволны. |
 |
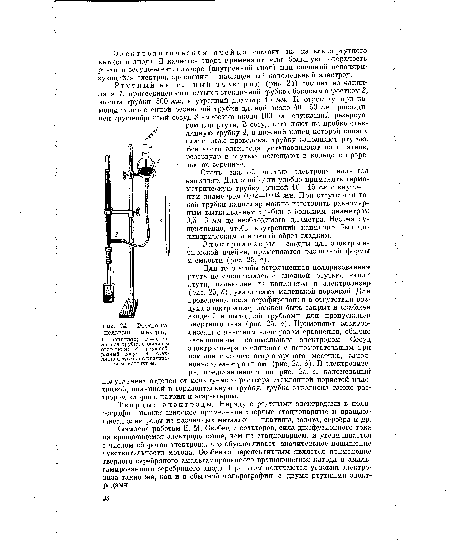
| Ртутно-капельный электрод. 1 — капилляр; 2 — стеклянная трубка с боковым отростком; 3 — грушеобразный сосуд; 4 — стеклянная трубка с платиновым контактом. |
 |