Полярографический метод анализа, предложенный .1. Неу-го гэку в 1922 г., относится к электрохимическим методам анализа. Сущность его заключается в получении зависимости силы тока от напряжения при электролизе растворов. Метод применим для исследования веществ, способных к электрохимическому окислению или восстановлению. Полярографический метод анализа отличается довольно высокой чувствительностью. Нижний предел определяемых концентраций составляет 10 5— 10-5 моль/л, а наиболее совершенными полярографами возможно определение до 10 8—10 9 моль/л. Обычная погрешность определения составляет 1—5 % [Барковский В. Ф. и др., 1972; Кац А. М., Контарович А. С., 1976].[ ...]
Теория и практика полярографического метода подробно освещены в ряде монографий. [Шевченко И. Т., Городыский В. И., 1964; Крюкова Т. Я. и др., 1969; Неугоу-эку Л., Ша Л., 1965].[ ...]
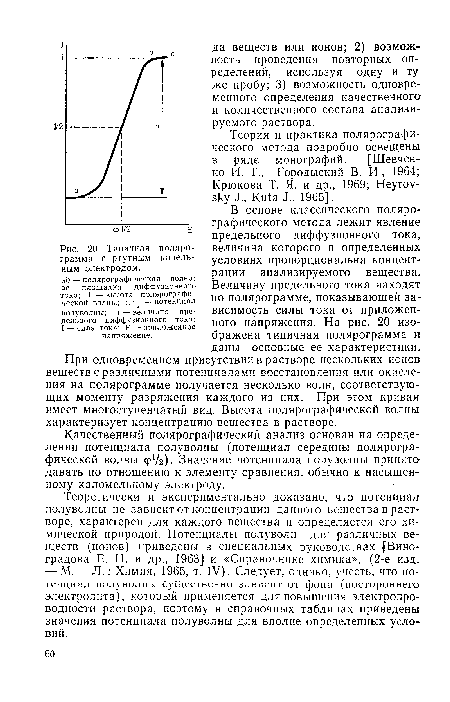
В основе классического полярографического метода лежит явление предельного диффузионного тока, величина которого в определенных условиях пропорциональна концентрации анализируемого вещества. Величину предельного тока находят по полярограмме, показывающей зависимость силы тока от приложенного напряжения. На рис. 20 изображена типичная полярограмма и даны основные ее характеристики.[ ...]
При одновременном присутствии в растворе нескольких ионов веществ с различными потенциалами восстановления или окисления на полярограмме получается несколько волн, соответствующих моменту разряжения каждого из них. При этом кривая имеет многоступенчатый вид. Высота полярографической волны характеризует концентрацию вещества в растворе.[ ...]
Качественный полярографический анализ основан на определении потенциала полуволны (потенциал середины полярографической волны ф7г). Значение потенциала полуволны принято давать по отношению к элементу сравнения, обычно к насыщенному каломельному электроду.[ ...]
Теоретически и экспериментально доказано, что потенциал полуволны не зависит от концентрации данного вещества в растворе, характерен для каждого вещества и определяется его химической природой. Потенциалы полуволн для различных веществ (ионов) приведены в специальных руководствах Виноградова Е. Н. и др., 1963] и «Справочнике химика», (2-е изд.[ ...]
В качестве фона применяют соли и щелочи одновалентных металлов, кислоты и др. Для определения щелочных металлов, обладающих отрицательным потенциалом восстановления, применяют тетраметиламмоний или его галоидные соли. Для определения органических веществ рекомендуют применять соли лития, тетраметиламмония и различные буферные растворы.[ ...]
Прилагаемое при полярографическом анализе напряжение охватывает область анодного окисления и катодного восстановления примерно от +1,3 до ■—1,6—2 В. Однако ртуть, используемая в катодной области, при высоких анодных потенциалах, применяемых, например, для изучения биологического окисления, не может быть использована вследствие ее анодного растворения уже при +0,3 В.[ ...]
На рис. 21 представлена схема полярографической установки. В полярографическую ячейку (3) погружены капельный ртутный микроэлектрод (1) и отвод насыщенного каломельного электрода сравнения (2). Питание подается с аккумуляторной батареи (4), напряжение которой приложено к концам реохорда (5). Реостат (6) служит для регулирования подаваемого на реохорд тока. Контроль напряжения производят по вольтметру (7). Образовавшуюся в результате электрохимического процесса силу тока измеряют гальванометром (8), чувствительность, которого можно регулировать шунтом (9). Ртуть в капилляр микроэлектрода (1) поступает из сосуда (10).[ ...]
Как видно из схемы, напряжение источника постоянного тока (4) поступает на электрод сравнения (плюс), и через «грушу» со ртутью — на ртутный микроэлектрод (минус). В установившемся режиме ртуть поступает в капилляр через соединительную трубку и продавливается силой собственной массы. Поляризующимся электродом является ртутный капельный электрод. Электрохимический процесс происходит до тех пор, пока образующаяся капля еще висит на конце капилляра. С отрывом капли процесс возобновляется на новой капле.[ ...]
Рисунки к данной главе:
| Типичная поляро-грамма с ртутным капельным электродом. |
 |
Аналогичные главы в дргуих документах:
| См. далее:Сущность метода |