Электроды, используемые для титрования кислот и оснований, являются индикаторными по отношению к концентрации ионов водорода. Мы рассмотрим два типа электродов: сурьмяный и стеклянный, которые, на наш взгляд, могут с успехом применяться в санитарно-химическом анализе для реакции нейтрализации и определения pH растворов.[ ...]
Сурьмяный электрод 5Ь/5Ь2Оя — электрод второго рода, составленный из металла и его малорастворимой окиси. Этот электрод используется для определения концентрации ионов водорода, так как металлический электрод в присутствии своего малорастворимого оксида выполняет функции водородного электрода.[ ...]
Недостаток сурьмяного электрода: не вполне обратимый электрод и измеряемые им потенциалы не вполне подчиняются уравнению Нернста.[ ...]
Кривые потенциометрического титрования реакции нейтрализации — изображение изменения pH раствора. Отдельные точки кривой титрования можно рассчитать по формулам для вычисления pH раствора соответствующих электролитов. При вычислении pH раствора сильных кислот или оснований, пренебрегая ионной силой раствора, концентрацию ионов Н или ОН можно приравнять к общей концентрации кислоты или щелочи.[ ...]
Электрод, опущенный в анализируемый раствор, должен быть индикаторным по отношению к концентрации ионов водорода. На поверхности такого электрода устанавливается равновесие: Н2 2Н+ - - 2е .[ ...]
При этом изменением объема в процессе титрования пренебрегают, так как это не оказывает существенного влияния на значения потенциалов и характеристики кривых.[ ...]
Рисунки к данной главе:
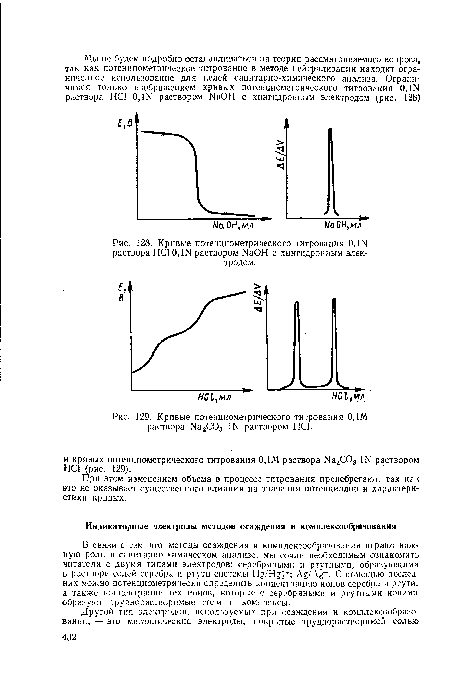
| Кривые потенциометрического титрования 0,Ш раствора НСЮ.Ш раствором №ОН с хингидронным электродом. |
 |