В состав почвообразующих пород и почв входят первичные и вторичные минералы. Первичные минералы слагают магматические породы, а в рыхлых породах и почвах являются остаточным материалом выветривания исходных пород. Вторичные минералы возникли из первичных под воздействием климатических и биологических факторов.[ ...]
Первичные минералы представлены преимущественно частицами больше 0,001 мм, вторичные — меньше 0,001 мм. В большинстве почв первичные минералы преобладают по массе над вторичными, за исключением ферраллитных почв, в которых первичных минералов часто меньше, чем вторичных.[ ...]
Так, в рыхлых породах больше кварца (5Ю2), как наиболее устойчивого к выветриванию минерала. Его содержание достигает 40—60 % и более. Второе место обычно занимают полевые шпаты (до 20 %), также обладающие большой механической прочностью, но менее устойчивые к химическому выветриванию. Среди них широко распространен ортоклаз (КА А). реже встречаются натриево-кальциевые полевые шпаты или плагиоклазы.[ ...]
Кварц и полевые шпаты крупнозернисты, поскольку выветривание их идет медленно. Они сосредоточены главным образом в песчаных и пылеватых частицах.[ ...]
Амфиболы, пироксены и многие слюды легко поддаются выветриванию, поэтому в рыхлых породах и почвах они содержатся в небольших количествах в виде мелких кристаллов.[ ...]
Устойчивость к выветриванию определяется природой минералов, их различием в химическом составе и кристаллической структуре. Рассматриваемые минералы, как большинство минеральных химических соединений, обладают структурами ионного типа, образованными противоположно заряженными ионами. Ионы в кристаллах минералов расположены в виде геометрически правильной пространственной решетки, называемой кристаллической. Благодаря такому строению кристаллы минералов имеют форму геометрически правильных многогранников. Для каждого минерала характерны своя кристаллическая решетка и определенная форма кристаллов.[ ...]
Взаимное расположение катионов и анионов в кристаллической решетке обусловливается их объемом или радиусами (ионы можно представить в виде сфер определенного радиуса). Число ионов противоположного знака, окружающих данный ион, называется координационным числом. Чем больше радиус иона, тем больше вокруг него может разместиться без взаимного соприкосновения противоположно заряженных ионов.[ ...]
Главным элементом структуры широко распространенных в почве кислородных соединений кремния является кремнекислородный тетраэдр (5Ю4)4-, в вершинах которого располагаются четыре иона кислорода, а в центре —■ ион кремния. Кремнекислородный тетраэдр обладает четырьмя свободными валентными связями, которые могут быть компенсированы присоединением катионов или соединением с другими кремнекислороднымп тетраэдрами.[ ...]
Тетраэдры, соединяясь через кислородные ионы, образуют различные сочетания или типы структур: островные, цепные, ленточные, листоватые (слоистые), каркасные. Каркасная структура распространена в полевых шпатах, кварце, цепная — в пироксенах, листоватая — в слюдах, глинистых минералах, ленточная — в амфиболах, островная — в оливине.[ ...]
В островной тип структуры входят кремнекислородные радикалы, состоящие из одного, двух и большего, но конечного числа тетраэдров. Изолированные тетраэдры соответствуют формуле радикала ¡О ,)4", спаренные — (31207)в , комплекс из трех тетраэдров — 3Оэ)в , из четырех — ¡Аг)8-, из шести — (5и018)12- (рис. 8).[ ...]
Рисунки к данной главе:
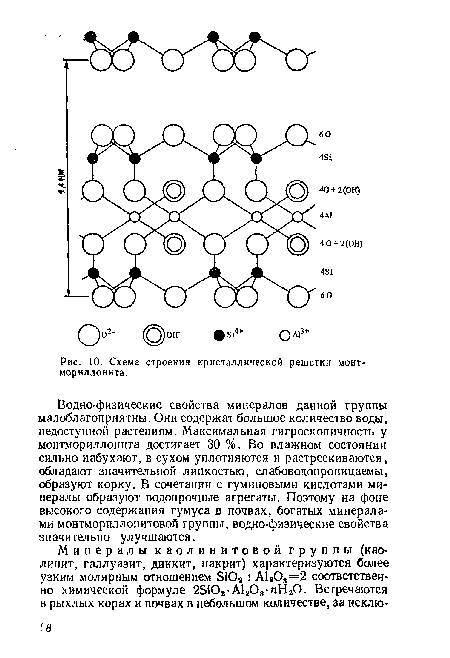
| Схема строения кристаллической решетки монтмориллонита. |
 |
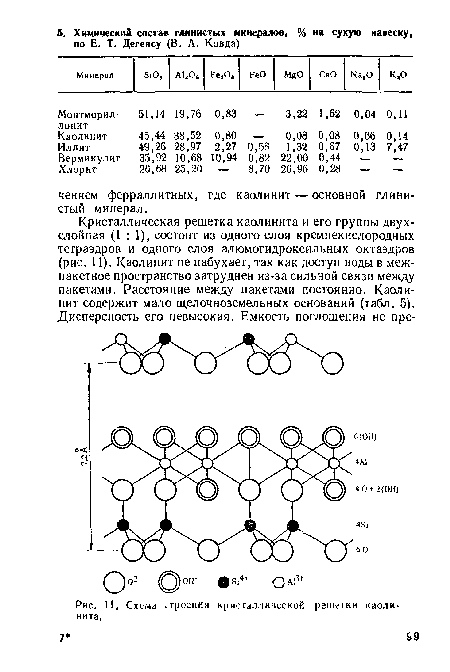
| Схеме! строения кристаллической решегки каолинита. |
 |