Константа гидролиза соли сильного основания и слабой кислоты равна ионному произведению воды, деленному на константу диссоциации слабой кислоты. Или, другими словами, константа гидролиза определяется по константе диссоциации слабой кислоты или слабого основания.[ ...]
Константа гидролиза связана с ионным произведением воды, константой диссоциации кислоты (основания) и степенью гидролиза зависимостями, приведенными в табл. 2.3.[ ...]
Константа гидролиза Кт характеризуется отношением ионного произведения воды к константе диссоциации кислоты КНА или основания /СМеОН.[ ...]
Диссоциация кремневой кислоты до ионов БЮз- в природной воде практически не происходит ввиду очень малого значения второй константы диссоциации (Кг = 1,6 ■ 10-12). При pH воды ниже 8 в ней присутствует лишь На5Ю3, обычно в коллоидном состоянии с частицами состава 5Ю2 • Н20 дали в виде поликремневой кислоты — х 8Ю2 ■ у Н20.[ ...]
В воде ионообменные смолы под влиянием осмотических явлений набухают. На этот процесс существенно влияет величина гидратации фиксированных ионов и про-тивоионов. Препятствуют набуханию смол частота и длина радикалов дивинилбензола, сшивающих длинные углеводородные цепи полимеров стирола с образованием трехмерной сетчатой структуры. Ясно, что чем больше степень сшивания полимерных цепей, тем более жесткую структуру имеет смола и тем меньше она набухает в водных растворах. Следует отметить, что область pH, в которой осуществляется обмен ионов, зависит от константы диссоциации ионообменных групп смолы. Так, сульфокислотные катиониты, например смола КУ 2 (р/(Лис < 1)> способны к обмену ионов водорода на другие катионы в широком интервале pH и при pH > 2,5—3 кислотность на обмен практически не влияет. Карбоксильные катиониты (р/Сдис = 5—6) обменивают свои ионы при pH > 7 и могут использоваться только в солевой форме. Катиониты, содержащие фенольные гидроксильные группы, способны к обмену лишь при pH > 8, т. е. в области значений pH, отвечающей диссоциации фенольных групп. Все это необходимо учитывать при выборе смол для очистки промышленных сточных вод.[ ...]
Значения констант диссоциации К и /Сг обратно пропорциональны ионной силе раствора, которая определяет активность рассматриваемых ионов. В то же время значения констант прямо пропорциональны температуре.[ ...]
Кислоты с константой диссоциации 10 7—10 9 умеренно гидролизованы при 20—40 °С и значительно гидролизуются при 100—■ 120°С и выше, что и делает возможным поглощение аммиака с получением растворов названных солей при обратимом процессе. Соли кислот с константами диссоциации ниже 10 9 более чем на 40% гидролизуются уже при 40°С. Процесс абсорбция аммиака растворами этих кислот мало отличается по условиям равновесия от абсорбции водой.[ ...]
Таким образом, в воде наряду с молекулами Н20 всегда присутствуют водные ионы. В табл. 50 представлены экспериментальные значения, характеризующие воду и лед как диссоциирующие среды. Из табл. 50 видно, что при плавлении на шесть порядков возрастает константа диссоциации молекулы Н20, на четыре порядка — постоянная скорости диссоциации и на два порядка уменьшается постоянная скорости рекомбинации.[ ...]
Первые измерения константы диссоциации молекулы НгО были выполнены Аррениусом (1890—1893). Он использовал свою теорию гидролиза и экспериментальные данные относительно гидролиза в растворах. Скорость гидролиза зависит от концентрации Н+ и ОН- ионов. Кольрауш оценил значение К н2о из данных по электропроводности чистой воды. Наиболее красивый метод определения постоянной диссоциации молекулы НгО был рассмотрен выше (Эйген и Майер, 1958).[ ...]
Все эти кислоты в воде — сильные электролиты и, следовательно, константа диссоциации каждой из них в водном растворе стремится к бесконечности. Вода — в данном случае нивелирующий силу кислот растворитель, уравнивающий их по силе. Иная картина в дифференцирующем силу кислот растворителе НАс. Серная кислота в этом растворителе в 40 раз слабее хлорной, а азотная кислота уступает хлорной в 250 раз.[ ...]
Величина pH сточной воды, при которой происходит обмен ионами, зависит от константы диссоциации ионообменных групп смолы. Сильнокислотные катиониты позволяют проводить процесс в любых средах, а слабокислотные - в щелочных и нейтральных. Так, катиониты с карбоксильными группами обмениваются ионами при рН>7, а с фенольными группами при рН>8.[ ...]
Для оценки изменения константы диссоциации воды в малых объемах определялись установившиеся значения концентрации стабильных ион-ра-дикалов в капле дистиллированной воды. С этой целью снималась кинетическая зависимость изменения концентрации радикалов в капле, выдерживаемой на тефлоновой подложке дозаторного устройства прибора ЛИК-2.[ ...]
В оборотной и сточной воде каждой концентрации ионов НС03- и Са2+ соответствует определенная концентрация растворенной С02, которая зависит от констант равновесия первой К2, и второй К2 ступеней диссоциации угольной кислоты, а также от константы произведения активностей (СаС03). Эта величина растворенной С02 называется «равновесной» углекислотой.[ ...]
Цианиды встречаются в водах в виде слабодиссоциированной, очень токсичной синильной кислоты и в виде также очень токсичных цианид-ионов. Отношение между концентрациями обеих этих форм определяется значением pH среды. Комплексные цианид-ионы в незначительной мере также диссоциируют с отделением ионов СЫ , Степень этой диссоциации выражается константами устойчивости, наибольшие значения ¡которых имеют комплексные цианиды железа ), железа(Ш) и кобальта, наименьшее — комплексный цианид цинка. Чем ниже константа устойчивости, тем больше выделяется ионов СЫ при диссоциации и, следовательно, тем токсичнее соединение.[ ...]
Например, вторая кажущаяся константа диссоциации (К2) карбоновой кислоты меняется от 4,2 -КН1 в пресной воде до 4,0 Ю-10 в воде, содержащей 9% хлора, и до 7,1. 10 10 в морской воде, содержащей 20% хлора, т. е. константа возрастает примерно в 20 раз [45].[ ...]
Относительное содержание в воде сероводорода (НгБ), гидросульфид- (НБ-) и сульфид-ионов (¿2-) зависит от величины pH воды и определяется расчетом при помощи констант диссоциации сероводородной кислоты. Ниже приведено содержание Нг5 в воде в зависимости от pH воды и общего количества соединений сероводорода при температуре 20°С.[ ...]
Далее по аналогии с разложением воды используется термин «разложение карбонатов». Уподобляя разложение карбонатов разложению воды, можно в то же время предполагать, что оно происходит легче, чем разложение воды (константа диссоциации НгО —Н+ + ОН порядка 1014, а константа диссоциации НСОз— Н+ + СО -порядка 108). Отсюда резкое повышение проникания карбонатов можно объяснить определенными условиями, которые предшествуют разложению воды. Если проникание через мембрану связано с метакарбонатами, нетрудно представить себе, как могут образоваться отложения карбоната кальция на поверхности мембраны. Подобный механизм позволяет объяснить образование отложений карбоната кальция и в отсутствии разложения воды.[ ...]
При данной температуре величина константы диссоциации остается постоянной, причем не только в воде, но и в любом водном растворе кислот, щелочей и солей. Поэтому при увеличении концентрации водородных ионов путем добавки кислоты соответственно уменьшается концентрация ионов гидроксила.[ ...]
Эллис и Андерсон показали [62], что константы диссоциации у кислот, например фосфорной и уксусной, которые при переходе из водной фазы в газовую не меняют своей структуры, слабо зависят от давления, а у кислот, переходящих в газовую фазу в форме ангидридов, например угольной, - сильно. Зависимость константы диссоциации сернистой кислоты от давления занимает промежуточное положение между указанными выше крайними случаями. По мнению авторов, этим подтверждаются данные о существовании сернистой кислоты в виде БОг • Н2О и о слабом взаимодействии оксида серы (IV) и воды.[ ...]
Проведенная в [24] оценка истинных констант диссоциации (Кс) с корректировкой концентрации Н250з на значения [Б02 своб.] и [ИБО ] показала, что их значения приблизительно в 2 раза больше Ка, а доля сернистой кислоты в форме Н2БОз составляет примерно 55-65 % всей массы растворенной в воде 502 и уменьшается с ростом температуры и содержания оксида серы (IV).[ ...]
Растворяющая способность тяжелой воды меньше, чем легкой. Для экзотермических реакций количество тепла, выделяемое в процессе реакции в 020, больше, чем в Н20, а при эндотермических реакциях тепла в результате реакции поглощается больше в 020, чем в Н20. Все процессы нейтрализации в тяжелой воде идут быстрее, а все процессы диссоциации в тяжелой воде происходят более медленно. Это связано с тем, что константа скорости рекомбинации больше в тяжелой воде, а постоянная скорости диссоциации больше в легкой воде (гл. 5).[ ...]
В приведенных формулах Ккмсл и Косн — константы диссоциации слабой кислоты и слабого основания; н2о — ионное произведение воды; Скисл, Сосн, Ссол — общая концентрация кислоты, основания и соли.[ ...]
Уравнения (3.94) — (3.96) совместно с уравнениями констант химического равновесия, записанными для ионов, участвующих в химических реакциях в объеме электролита (уравнения произведения растворимостей, констант нестойкости комплексных ионов, ионного произведения воды, констант диссоциаций), описывают изменение pH среды с разделением продуктов электродных реакций. Модель учитывает начальную концентрацию веществ в обрабатываемом растворе, объемы анодного и катодного пространства, миграцию веществ через неактивную диафрагму при изменяющихся числах переноса, химические превращения веществ на электродах и в объеме электролита.[ ...]
КМЦ — слабая кислота; при степени замещения 0,8 константа диссоциации КМЦ равна 5-10-5. Соли КМЦ тяжелых и поливалентных металлов, включай А1, нерастворимы в воде. Вязкость растворов Иа-КМи зависит от pH (максимум г соответствует pH = 6-4-9), с повышением температуры, особенно выше 50 °С, происходит необратимое уменьшение вязкости — диспергирование надмолекулярных структур Ыа-КМЦ.[ ...]
Химические свойства. Диоксид серы, растворяясь в воде, образует сернистую кислоту Н3503 с константами диссоциации: Кх = 1,7-10-2, /(2 = 6,2-10-8. Окислители переводят БОа в Э03 или Н28 04, под действием восстановителей, в зависимости от их эффективности, Б02 превращается либо в элементарную серу (например, Н28 в печи Клауса), либо в Н28 [например, хлорид олова (II) или фосфорноватая кислота].[ ...]
Содержание различных форм сернистых соединений в воде, диссоциированных согласно приведенным ниже уравнениям, определяется по константам диссоциации сероводородной кислоты первой и второй ступени [23].[ ...]
 |
| Модель основных химических равновесий компонентов воды и состояния насыщения ее карбонатом кальция | 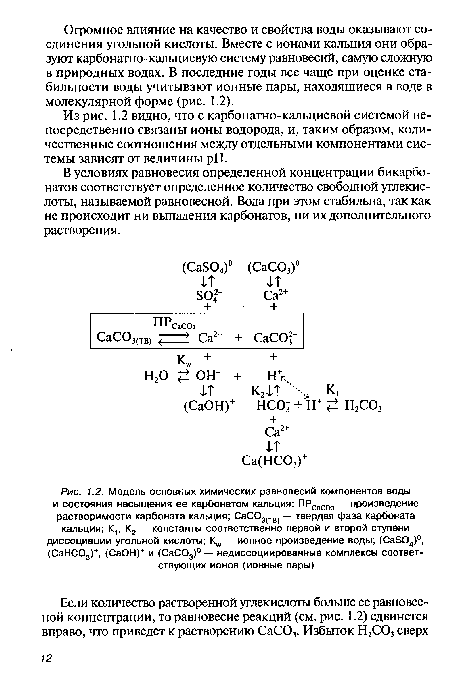 |
Равновесие нейтрализации пиридиновых оснований кислотами с константой диссоциации менее 10 5 настолько сдвинуто в сторону обратной реакции, что условия улавливания не будут отличаться от условий поглощения водой.[ ...]
Дифференцирующее действие растворителей — увеличение разности между константами электролитической диссоциации электролитов в данном растворителе по сравнению со стандартным (в качестве последнего чаще всего выбирается вода) (стр. 49 сл.).[ ...]
Основные физические свойства. Температура кипения —78,5 °С. Растворимость в воде: в 100 мл воды при 20 °С и 760 мм рт. ст. растворяется 88 мл С02. Константы диссоциации: Кг = 4,3-10 7, Кг = 5,6-10"11.[ ...]
В случае сильных электролитов (к ним могут быть отнесены все растворенные в природной воде соли), в связи с отклонениями свойств их растворов от идеальных, для которых создана классическая теория электролитической диссоциации, при вычислении констант диссоциации необходимо использовать активности или умножать аналитически определяемые концентрации ионов на соответствующие коэффициенты активности.[ ...]
Оказалось, что при связывании аналога ЭПР-сигнал заметно уширяется, а скорость продольной релаксации воды возрастает. В алкогольдегидрогеназе печени лошади титровались с помощью аналога 2-го участка на поверхности фермента с константной диссоциации комплекса Кд= 17+8 мкМ и 5—6 участков с Кд = 9 мкМ. Константа диссоциации НАДН из комплекса с ферментом, определенная при титровании, составила 5-10 5М, что значительно превышает величину, найденную ранее методом флюориметрического титрования—-2,0 • 10“7М [165].[ ...]
Константа диссоциации 2М-4Х составляет 5,4 -10“4. Чистая 2М-4Х практически не имеет запаха [15], технические препараты в большинстве случаев имеют неприятный запах хлоркрезолов. С целью очистки и получения 2М-4Х, пригодной для аналитических целей, ее несколько раз перекристаллизовывают из бензола или хлорбензола [5].[ ...]
Важно подчеркнуть, что в реакциях нейтрализации ОН-, образующихся при растворении карбонатов и силикатов, участвуют не только угольная кислота, но и органические кислоты (особенно фульво- и гуминовые), являющиеся агентом интенсивного разложения пород. Сильная диссоциация многих органических кислот приводит к увеличению в воде концентраций Н . Константы диссоциации таких распространенных в природе соединений, как фульво- и гуминовые кислоты, приближаются к и-10-3-«• 10"5. Это означает, что они могут снижать pH реальных подземных вод до 3 и менее. В связи с зтим такие органические кислоты интенсивно разлагают силикаты с разрушением их кристаллической решетки. Степень такого разложения тем больше, чем ниже минерализация подземных вод и чем более кислыми они являются.[ ...]
Эти равновесия осложняются медленным превращением гипохлорита в хлорид и хлорат, с происходящим в результате этого уменьшением активного хлора для отбелки. Знание того [344], что константа гидролиза хлора в воде равна 4.5ХЮ-4, а константа диссоциации хлорноватистой кислоты [345, 346, 347] около 4ХЮ 8, создает возможность-путем вычисления определить, что составы разбавленных растворов, употребляемых на практике (содержащих больше или меньше 0,8 % активного хлора) меняются в зависимости от pH, как указано ранее. Свыше 95% активного хлора существует в виде недиссоциированной хлорноватистой кислоты в пределах рНотЗ до 6; при pH 9 около 97% присутствует в качестве иона гипохлорита, а в кислом растворе при pH 2 гидролиз дает около 32% активного хлора [82]. То, что скорость, при которой целлюлоза восстанавливает 0,04 н. гипохлорит натрия больше примерно в 10 раз при pH 7, чем при pH 4,6 или pH 9, говорит о том, что иедиссоциированная хлорноватистая кислота легче окисляет целлюлозу, чем ион гипохлорита или активный хлор [66, 84, 348]. Более медленная реакция в кислом растворе сильно катализируется ярким дневным светом [79], реакция при pH 7—ультрафиолетовыми линиями в ртутном спектре [341], а окисление в каустической соде мерсеризующей концентрации, также является быстрым [66]. В результате этих окислений из отбеливаемых примесей образуются слабые органические кислоты, а из слабой хлорноватистой кислоты — сильная соляная кислота. Следовательно, щелочная белильная жидкость во время использования имеет тенденцию приблизиться к опасным пределам pH от 6 до 8, где переокисление, ведущее к деградации целлюлозы, происходит быстро [345]. Вследствие этого было тщательно изучено [345] как с теоретической [82], так и с практической [83] точек зрения, буферное действие присутствующего натриевого или кальциевого основания вместе с эффективностью добавления карбоната натрия или кальция, бората натрия, фосфатов, ацетата, цинкового и алюминиевого буферов. Однако отбелка может быть безопасно и быстро выполнена вблизи нейтральной точки при соблюдении некоторых определенных условий [83].[ ...]
В химическом отношении селен является аналогом серы, находясь с ней в главной подгруппе VI группы элементов. Для селена характерны степени окисления — 2, + 4, + 6; он образует диоксид Se02 и триоксид Se03, соответственно селенистую H2Se03 и селеновую кислоты H2Se04 (соли — селениты и селенаты). Селенистая кислота слабая, ее константы диссоциации: Кх = 2 ■ 10 3 и К2 = 5 ■ 10 9. Селеновая кислота сильная, степень ее диссоциации близка к степени диссоциации серной кислоты. Селениты щелочных металлов хорошо растворимы, другие селениты имеют низкую растворимость. Селенаты, как правило, хорошо растворимы в воде. Для содержания селенатов в воде установлен ПДК 0,2 мг/м3 в расчете на селен. Соли слабой селеноводородной кислоты H2Se — селениды — сходны по свойствам с сульфидами.[ ...]
Для осуществления реакции конденсации необходим достаточно сильный катализатор. Целлюлоза обратимо адсорбирует формальдегид из нейтральных водных растворов [14], причем скорость адсорбции увеличивается в 2 раза при добавлении к реакционному раствору 5% нейтральной соли, такой, как, например, хлорид калия [15]. Однако реакция конденсации протекает только в кислой среде. Показано [16], что продукты конденсации, устойчивые к обработке в кипящей воде (pH 7), образуются только при использовании в качестве катализаторов кислот с константой диссоциации 10 2 и выше. Позже эти реакции были осуществлены в присутствии достаточно эффективного катализатора — кислот, константа диссоциации которых ниже 10 3 и 10 4 (например, молочной и винной кислот) [17].[ ...]