Дезаминирование—потеря аминокислотами аминогруппы, ведущая к распаду аминокислоты.[ ...]
Дезаминирование — процесс ферментативного удаления аминогрупп из аминокислот.[ ...]
Реакция дезаминирования протекает с участием моноаминооксидаз или диаминооксидаз - медьсодержащих ферментов в реакционный центр пиридоксоль и (или) флавин. Эти ферменты, ответственные за быструю утилизацию катехоламинов, сосредоточены в митохондриях животных.[ ...]
| Окислительно« дезаминирование азотистой кислотой цитозина в урацил. | 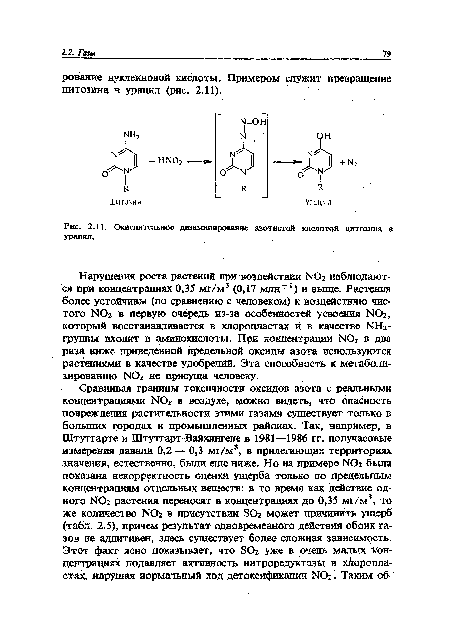 |
| Ступенчатое деметилирование, дезаминирование и декарбок-силирование гербицида хлороксурона под влиянием смешанной культуры почвенных микроорганизмов. | 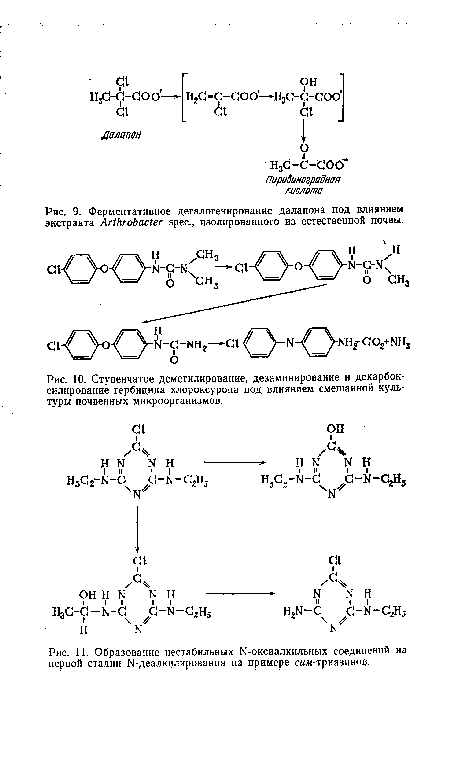 |
Этот путь лишь предполагается.[ ...]
Вероятный путь катаболизма гистамина у растений - дезаминирование с участием моноамино- и диаминооксидаз, поскольку у них присутствуют указанные ферменты.[ ...]
В растениях фермент, участвующий в реакции окислительного дезаминирования, был впервые обнаружен в проростках разных видов растений и идентифицирован как диаминооксидаза. Экстракты из Trifolium pratense и Т. repens были способны в качестве субстратов использовать норадреналин и другие моноамины. В дальнейшем было показано, что не все диаминооксидазы способны утилизировать биогенные моноамины.[ ...]
| 8.2 | ![Изменение взаимодействия оснований нуклеиновых кислот после дезаминирования или ионизации (в скобках — основание, образующее пару) [5]](/static/pngsmall/826765328.png) |
Имеется несколько путей трансформации аминопроизводных бензола (анилина). Один из них связан с окислительным дезаминированием и образованием фенолов, последующая судьба которых описана выше (Kaufman, 1975). Второй представляет реакцию ацетилирования, в результате которой образуются ацетанилиды. Реакция обратима: деацетилирование вновь ведет к накоплению анилинов в среде (Суровцева, 1979). Третий путь заключается в последовательном окислении аминогруппы до гидроксиламина и нитробензола. При определенных обстоятельствах эта реакция в культуре микроорганизмов также обратима. Четвертый путь представляет собой реакцию конденсации анилинов и некоторых продуктов их окисления до азобензолов и других высокомолекулярных полимеров (Kaufman, 1975; Bartha, 1975).[ ...]
ВТМ, причем в основе механизма инактивации лежит, по-видимому, тот же процесс, что и при мутагенном действии, а именно дезаминирование оснований. Мягкие условия обработки незначительно влияют на серологическую активность вируса, однако содержание аминогрупп в белке может при этом снижаться. При более жестких условиях вирусная частица разрушается.[ ...]
В табл. 5.9 приводятся некоторые данные о присутствии у ряда видов растений диаминооксидаз, катализирующих окислительное дезаминирование гистамина и некоторых биогенных моноаминов; они обнаружены у 21 вида из 7 семейств. Фермент впервые был выделен и очищен из проростков гороха Pisum sativum.[ ...]
Для того чтобы амиды образовались, необходима затрата энергии (АТФ) и присутствие ионов магния.[ ...]
Катаболизм серотонина в растениях направлен либо на метилирование с помощью триктофанметилтрансферазы (ТМТ), либо на окислительное дезаминирование с участием моноаминооксидазы (МАО) (рис. 1.7).[ ...]
Индолилацетальдегид может образовываться не только путем декарбоксилирования индолилпировиноградной кислоты, но и при окислительном дезаминировании трип-тамина, который, например, в опытах с колеоптилями овса и побегами гороха в существенных количествах превращается в ИУК. Однако пути образования самого триптамина в растениях еще не вполне ясны.[ ...]
Из 24 перечисленных здесь азотистых мутантов ВТМ 23 согласуются с постулированным механизмом мутагенного действия азотистой кислоты, т. е. дезаминированном цитозина в урацил и аденина в гипоксантип (последнее соединение участвует в спаривании подобно гуанину, что приводит к замене аденина гуанином). Исключение составляет штамм РМ2,в структурном белке которого глутаминовая кислота (ГАД) замещена па аспарагиновую кислоту (ГАУ). Возможно, штамм РМ2 возник не под действием азотистой кислоты, а спонтанно. Недавно был описан еще один азотистый мутант РМ5 1707], в структурном белке которого аргинин в положении 112 замещен цистеином. Это замещение могло произойти в результате одного пз двух изменений: ЦГЦ УГЦ или ЦГУ-»-УГУ.[ ...]
Бактерии с помощью протеаз гидролитически расщепляют соответствующие азотсодержащие органические соединения до аминокислот, кеторые подвергаются дальнейшим превращениям — дезаминированию, декарбоксилированию и т. д. Природа образующихся продуктов зависит от условий и характера процессов, при которых идет дезаминирование (прямое, окислительное, восстановительное) и декарбоксилирование в аэротенках и метантенках.[ ...]
Скорость конденсации меламиновых смол зависит от многих факторов: pH, молярного соотношения реагентов, наличия соединений, замедляющих конденсацию, например метанола, наличия продуктов гидролиза или дезаминирования меламина в реакционной смеси, солей.[ ...]
Ферменты катаболизма биогенных аминов. Как уже отмечалось, катаболизм биогенных аминов происходит с участием двух основных ферментов - аминооксидаз и метилтрансфераз. У животных реакции окислительного дезаминирования протекают с участием моноамино-оксидаз, а в ряде случаев и диаминооксидаз. Оба типа ферментов являются медьсодержащими белками и катализируют преимущественно распад моноаминов или диаминов.[ ...]
Химическое описание процессов обмена веществ в организме рыбы еще не дает нам представления об их биологическом значении. Например, химические процессы распада гликогена с образованием сахара или процесс дезаминирования одинаково протекаю? как в случае, когда они являются энергетическим источником при совершаемой мышечной работе, так и в случае образования новых клеток или замены, восстановления составных частей в них.[ ...]
Поступившие в организм вредные химические вещества подвергаются разнообразным превращениям, почти все органические вещества вступают в различные химические реакции: окисления, восстановления, гидролиза, дезаминирования, метилирования, ацетилирования, образования парных соединений с некоторыми кислотами. Не подвергаются превращениям только химически инертные вещества, например, бензин, который выделяется из организма в неизменном виде.[ ...]
Попавшие в кровь посторонние вещества разносятся по организму и достигают различных органов и систем, где они и подвергаются различным биологическим и химическим превращениям (окисЛение, гидролитическое расщепление, дезаминирование, восстановление, образование парных соединений и т. д,). В результате видоизменений химические вещества в основном превращаются в менее токсичные соединения, т. е. обезвреживаются и только в некоторых случаях они переходят в более токсичные.[ ...]
Физиологическая роль названных амидов выяснена классическими работами Д. Н. Прянишникова. Установлено, что в результате образования аспарагина и глютамина происходит обезвреживание аммиака, накапливающегося в высших растениях при дезаминировании аминокислот или обильном аммиачном питании при недостатке у растений углеводов.[ ...]
При экспозиции растений в темноте в отсутствие сахаров нового синтеза белка и его обновления не происходит [8]. В этих условиях происходит только непрерывный распад белка до аминокислот, а при более длительной экспозиции растений в темноте происходит дезаминирование аминокислот с образованием в качестве продукта их распада — аммиака. Одновременно с распадом белка происходит и распад хлорофилла. Это можно видеть из данных таблицы 3.[ ...]
Два последних соединения и ванилиновый альдегид являются обычными продуктами метаболизма растений, поэтому не исключено, что указанная схема применима и к растениям. В отличие от животных моноаминооксидазы, хотя и присутствуют в растениях, но играют меньшую роль в окислительном дезаминировании катехоламинов, чем диа-минооксидазы.[ ...]
В зависимости от специфичности к субстрату различают А- и В-типы моноаминооксидаз. А-тип преимущественно использует адреналин, норадреналин и серотонин, тогда как В-тип - другие моноамины, в том числе триптамин и метилгистамин. Оба типа фермента в равной мере и с высокой скоростью катализируют дезаминирование и окисление тирамина и дофамина. Скорость реакций с участием моноаминооксидаз зависит от pH.[ ...]
Таким образом, сера играет важную роль в углеводном и азотном обмене в растениях.[ ...]
Значительную роль при ароматизации ациклических соединений играют фенилпир овин оградные кислоты - как первичные ароматические продукты - и ароматические аминокислоты - фенилаланин и тирозин. Для этих аминокислот характерны два типа реакций - декар-боксилирование, ведущее к образованию алкалоидов, и дезаминирование, приводящее к коричной кислоте и ее производным, из которых далее образуются многие растительные фенольные соединения, как схематически изображено на рис. 11.[ ...]
Разложение азотсодержащих веществ (белков) протекает в два этапа. На первом под влиянием аэробных и анаэробных микроорганизмов белки расщепляются с выделением содержащегося в них азота в виде МНз (стадия аммонификации) и образованием пептонов (продуктов первичного распада белков), а затем аминокислот. Последующее окислительное и восстановительное дезаминирование и декарбок-силированне приводят к полному распаду пептонов и аминокислот. Длительность первого этапа составляет от одного до нескольких лет. На втором этапе ЫНз окисляется сначала до Н1 02, а затем до НЫОз. Окончательное возвращение азота в атмосферу происходит под действием бактерий — денитрификаторов, которые разлагают нитраты молекулярного азота. Продолжительность периода минерализации составляет 30-40 лет и более.[ ...]
В принципе представляется возможным индуцировать мутации вирусов путем обработки вирусной РНК ферментами, изменяющими функциональные группы пуриновых и пиримидиновых оснований, но не действующими; на фосфодиэфирные связи. Несмотря на то что фермент участвовал в дезаминировании аденозино-вых остатков в деградированной РНК, он не оказывал видимого действия на интактную молекулу РНК ВТМ, о чем можно было судить по отсутствии мутантов.[ ...]
Анаэробное разложение белков вызывается спорообразующими палочками: Bacillus putrificus, Bacillus sporogenes. Разложение белковых соединений вызывается и факультативными анаэробами Proteus vulgaris, Bacteria coli. Степень и интенсивность разложения белковых соединений зависит от химической структуры белка и вида микроорганизмов. Аминокислоты, образующиеся в процессе распада белков в анаэробных условиях, подвергаются восстановительному дезаминированию с образованием предельных органических кислот и аммиака. Органические кислоты могут разлагаться с образованием метана и диоксида углерода. Продуктами аммонификации в анаэробных условиях будут метан, аммиак и диоксид углерода.[ ...]
Янтарная кислота, образовавшаяся в цикле Кребса, дает основу для.образования порфиринового ядра хлорофилла. Поскольку имеется ряд реакций и процессов, благодаря которым отдельные компоненты извлекаются из цикла Кребса, должны быть и обратные процессы, поставляющие их в цикл. Если бы этого не было, скорость превращения в аэробной фазе дыхания заметно бы снизилась. Такими реакциями является окислительное дезаминирование аминокислот, приводящее к образованию органических кислот.[ ...]
Генные мутации заключаются в изменениях индивидуальных генов. Поэтому их еще называют точечными мутациями и классифицируют на односайтовые и многосайтовые. Односайтовая мутация затрагивает один сайт, многосайтовая — несколько сайтов генного локуса. Некоторые сайты являются «горячими точками», т. к. в них происходят концентрированные мутации, что связано с наличием в нуклеотидных последовательностях модифицированных оснований. Последние подвергаются частому дезаминированию, а это ведет к изменениям в последовательностях оснований.[ ...]
Обнаружено, что пуриновые основания свободной РНК ВТМ взаимодействуют с азотистой кислотой чаще, чем цитозин (примерно па 50%). Однако при обработке интактных частиц дело обстоит по-иному. При некоторых условиях интактные вирусные частицы инактивируются азотистой кислотой значительно медленнее, чем свободная РНК, и при этом остатки гуанина не вступают в реакцию [1513]. Цитозин РНК в составе интактных частиц дезаминируется в 1,8 раза быстрее, чем аденин, тогда как скорость дезаминирования цитозина в составе свободной РНК составляет 0,7 скорости дезаминирования аденина.[ ...]
Однако, оказалось, что разложение тетрафторборатов в растворителях, содержащих карбонильные, амидные, спиртовые группы и способных быть донорами протона, может служить препаративным методом неводного дезаминирования ароматических аминов. Арилфториды в продуктах реакции не обнаруживались.[ ...]
Теоретически представляется возможным, что в процессе синтеза вирусного белка in. vivo считываться могут либо плюс-цепи РНК, либо минус-цепи (у которых последовательность оснований комплементарна последовательности оснований РНК вириона). Частота некоторых замещений аминокислот с несомненностью свидетельствует, что в роли матрицы при синтезе белка выступает РНК вириона, а не комплементарная ей минус-цепь [1923]. Так, фенилаланин (УУУ или У УД) часто замещает другие аминокислоты в структурном белке азотистых мутантов ВТМ, однако не обнаружено ни одного азотистого мутанта, в белке которого фенилаланин был бы замощен другой аминокислотой, так как ни УУУ, ни УУЦ при дезаминировании не дают триплета, кодирующего какую-либо другую аминокислоту. Результат был бы. противоположным, если бы роль матрицы играла минус-цоль, поскольку известно, что первичное мутационное событие совершается в шгае-цепи РНК, обработанной мутагеном. Если бы матричную функцию действительно выполняла минус-цень, то соответствующий комплементарный триплет для фенилаланина в РНК вириона (ААА) в результате дезаминирования превращался бы в триплеты, кодирующие другие аминокислоты, которые в этом случае могли бы замещать фенилаланин в структурном белке.[ ...]
Процесс самообновления белка играет фундаментальную роль в органическом мире. Для поддержания прижизненного состояния биологических структур необходима постоянная затрата энергии. Источником энергии в белковых структурных элементах организмов может служить непрерывное окисление входящих в состав белка аминокислот. Взамен окислившихся аминокислот в белковую молекулу включаются новые аминокислоты, чем и обеспечивается сохранение постоянства состава белка. Освобождающиеся в процессе окисления аминокислот безазотистые остатки вовлекаются в общий обмен веществ в растении и, взаимодействуя с поступающим извне или образующимся в самом растении аммиаком (при дезаминировании аминокислот), могут давать новые аминокислоты.[ ...]
Сивушные масла состоят в основном из высших спиртов с примесью других веществ — кислот, фенолов, терпенов. Состав различных образцов сивушного масла непостоянен, а зависит от содержания в сусле азотистых веществ и формы, в которой они присутствуют. Сивушные масла получаются при ректификации гидролизного спирта, выход равен 0,3—0,7% от количества спирта. Чаще встречаются в сивушном масле следующие спирты: амиловый, изоамиловый, изобутиловый, пропиловый. Источником спиртов сивушного масла являются аминокислоты, находящиеся в питательной среде или образующиеся при автолизе или гидролизе дрожжевого белка. В процессе азотистого питания дрожжей белки расщепляются до аминокислот; затем в результате гидролитического дезаминирования последних, т. е. отщепления амин-ной группы ЫН2, и декарбоксилирования (отщепление СО2) образуются высшие спирты, входящие в состав сивушного масла.[ ...]
Такие изменения in vitro можно вызвать действием различных химических реагентов при соответствующим образом контролируемых условиях, примером чего может служить дезаминирование некоторых осповапий под действием азотистой кислоты.[ ...]
Роль сахаров в процессе лигнификации выяснилась в последние годы. Исследованиями с меченой глюкозой древесины сосны Pinus strobus и Eucalyptus nitens /27, 28/ был подтвержден механизм образования лигнина через шикимовую (см. рис. 2) и префеновую (рис. 3) кислоты. Аналогичные эксперименты с меченой шикимовой кислотой подтвердили, что этот механизм является при лигнификации решающим. Ацетатный механизм (см. рис. 1) в процессе лигнификации не играет роли. Шикимовая кислота чрезвычайно распространена в высших растениях,и в настоящее время установлено, что шикимовая и префеновая кислоты управляют синтезом ароматических соединений в микроорганизмах и растениях. Далее было установлено, что ключевую роль при образовании лигнина играют аромаэтнеские аминокио-лоты - фенилаланин и тирозин, которые являются промежуточными продуктами метаболизма фенилпропаноидов (рис. 5). Опыты с мечеными фенилаланином и тирозином однозначно доказали, что все растения обладают способностью инкорпорировать фенилаланин в ароматической части лигнина. С другой стороны, тирозин не играет такой универсальной роли в процессе лигнификации растений. Поэтому предпочтительным оказывается механизм с участием фенилаланина, превращаемого дезаминированием в коричную кислоту (рис. 6), а не сходный механизм перехода тирозина в n-кумаровую кислоту.[ ...]