Константы уравнения Фрейндлиха для различных органических веществ при адсорбции из водных растворов активными углями марок КАД и ОУ приведены в работе [425].[ ...]
В отличие от уравнения Фрейндлиха уравнение Ленгмюра охватывает весь диапазон концентраций от нуля до насыщения.[ ...]
Графическая форма уравнения Фрейндлиха представлена на рис. 11.15. Как видно из рисунка, существует линейная зависимость логарифма времени до проскока от логарифма концентрации сорбируемого соединения. Эта линия имеет наклон (Ь=1ёа) а соответствует отрезку, отсекаемому этой линией на оси ординат (например, ОА). Кроме того (как следует из этого же рисунка), правая часть уравнения (11.24) уменьшается при увеличении влажности анализируемого воздуха в случае концентрирования микропримесей токсичных веществ. В результате уменьшается т, т. е. уменьшается объем до проскока и понижается эффективность сорбента.[ ...]
| 9.5 | 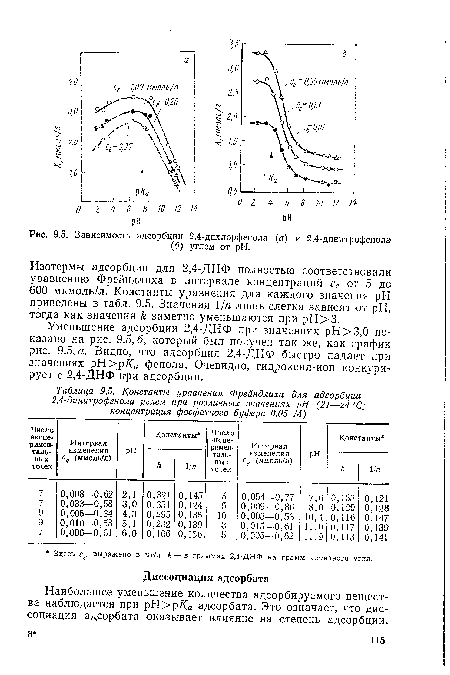 |
Показатель степени в уравнении Фрейндлиха выражает крутизну кривой. Чем п больше, тем круче растет изотерма. Следовательно, данное вещество лучше адсорбируется из раствора, и расход адсорбента для его извлечения потребуется меньший.[ ...]
При адсорбции из водных растворов уравнение Ленгмюра наиболее пригодно в тех случаях, когда адсорбируются большие молекулы, например молекулы гумусовых веществ, обусловливающие окраску природных вод. При адсорбции меньших молекул, обычно даже при больших равновесных концентрациях, удельная адсорбция не достигает предела, а постепенно, хотя и медленно, продолжает изменяться. При этом условия адсорбционного равновесия хорошо выражаются эмпирическим уравнением Фрейндлиха Г = = аС1/к (уравнение параболы), гдеа и Мк — константы, определяющие кривизну параболы.[ ...]
Сорбция радия происходит в соответствии с уравнением Фрейндлиха. В целом сорбция радия на вторичных минералах значительно более интенсивна, чем сорбция урана.[ ...]
Изотермы адсорбции для 2,4-ДНФ полностью соответствовали уравнению Фрейндлиха в интервале концентраций се от 5 до 600 мкмоль/л. Константы уравнения для каждого значения pH приведены в табл. 9.5. Значения 1 /п лишь слегка зависят от pH, тогда как значения заметно уменьшаются при рН>3.[ ...]
Поскольку весь интервал данных не может быть полностью описан нв уравнением Фрейндлиха, ни уравнением Ленгмюра, пытались использовать то уравнение, которое более соответствовало оцениваемой части экспериментальных данных. Если последние не могли быть описаны ни той, ни другой изотермой, данные сравнивались без помощи уравнений. Использование уравнений Ленгмюра и Фрейндлиха для описания равновесия процесса адсорбций фенолов подробно обсуждено в [12].[ ...]
Экспериментальные данные для 2,4-ДХФ очень хорошо описывались адсорбционной изотермой Фрейндлиха. С помощью регрессионного анализа были определены константы уравнения, представленные в табл. 9.4. Значения и 1/п примерно постоянны в интервале pH = 2—8,3. Однако отмечено увеличение 1/п и уменьшение к при изменении pH в интервале 8,3—11,7.[ ...]
Для описания молекулярной адсорбции в случае разбавленных растворов обычно применяются эмпирическое уравнение Фрейндлиха и уравнение Лэнгмюра, рассматриваемые в курсе коллоидной химии (Воюцкий, 1964).[ ...]
Такие биологические объекты, как бактерии и вирусы, несмотря на крупные размеры, хорошо сорбируются АУ. Изотерма сорбции E. Coli описывается уравнением Лэнгмюра, а вируса Polio — уравнением Фрейндлиха.[ ...]
Адсорбция на активном угле пестицидов разных классов, в том числе фосфамида и карбофоса, детально рассмотрена в работе [29].[ ...]
Зависимость адсорбции 2,4-ДХФ от pH раствора наиболее полно представлена на рис. 9.5, а. Было вычислено также количество адсорбированного вещества путем подстановки значений се в уравнения Фрейндлиха для каждого pH.[ ...]
Закономерности адсорбции ПАУ как неполярных гидрофобных соединений различными минеральными и органическими частицами полностью не изучены. Многие авторы показали, что для различных ПАУ адсорбция может быть описана уравнением Фрейндлиха, причем коэффициент 1/и « 1, т. е. это линейная зависимость между количеством адсорбированного вещества и его равновесной концентрацией. Сорбционная способность в значительной мере зависит от уровня растворимости ароматического соединения.[ ...]
Изотермы сорбции (рис. Сорбционная емкость ЛАУ при высоких равновесных концентрациях (Ср 300 мг/дм3) достигает Г = 250—500 мг/г, что значительно выше, чем при доочистке многих других видов сточных вод на углях АГ-3, АГ-5, КАД и АА. Следует отметить, что емкость полидисперсных ЛАУ в 2—3 раза выше, чем гранулированных.[ ...]
Многие авторы полагают, что в основе механизма удаления вирусов коагуляцией лежит процесс комплексообразования трехвалентных металлов с ионизированными группами протеинов [192 — 195]. Вместе с. тем показано, что для описания процесса ассоциации вирусов с продуктами гидролиза коагулянтов применимо уравнение адсорбции Фрейндлиха [192].[ ...]
Наряду с концепцией о прямом химическом взаимодействии ПАВ с добавленными к воде соединениями, нельзя не учитывать физической адсорбции. Показано, в частности, что продукты гидролиза коагулянта одинаково эффективны как при удалении анионных, так и неионогенных ПАВ, а закономерности удаления АС и АБС могут быть описаны уравнением физической адсорбции [67]. Возможность использования выражения Фрейндлиха для количественной оценки сорбции моющего средства ОП-7 на осадках AI(OH)3, Fe(OH)3 и Mg(OH)2 при pH > 6 доказана Хрусталевым и др. [90].[ ...]
Хотя зависимости А? от температуры для ИКБ-4, ИКБ-6 имеют линейный характер, на значения заметно влияет концентрация ингибитора в растворе (рис.2,3). С целью определения зависимости £ от концентрации ингибитора нами в данной работе были сняты изотермы адсорбции в широком диапазоне концентраций. Для описания изотерм адсорбции обычно используют уравнения изотерм Леншюра, Темкина, Фрейндлиха, Фрумкина и др., описанные б работах С4,5 1, которые устанавливают зависимость количества адсорбированного вещества от его концентрации.[ ...]
Чтобы удостовериться, что эти данные обоснованны для широкого интервала концентраций, были получены изотермы адсорбции 2,4-ДХФ для каждого из восьми размеров частиц адсорбента. Интервал равновесных концентраций адсорбата в этих экспериментах составил 0,01—2,0 ммоль/л. Сверх этого интервала экспериментальные данные были экстраполированы как прямая линия, исходя из уравнения Фрейндлиха, причем константы для этого были определены по методу наименьших квадратов.[ ...]
Для установления равновесия жидкой и твердой фаз (рис. 8.5.1) жидкость постепенно, небольшими порциями приводится в соприкосновение с сорбентом. Масса вещества, перешедшего на сорбент, определяется как разность исходной и остаточной концентрации этого вещества в жидкой фазе. Равновесное состояние является функцией свойств используемого сорбента, состава отходящей воды или газа и, очевидно, температуры и концентрации в растворе ионов водорода (pH). Для получения более полной картины равновесного состояния можно использовать уравнения, описывающие процесс сорбирования из растворов с одним растворенным веществом, например изотерма Лангмюра qe — kcj(1 + bc) или изотерма Фрейндлиха qe = kc]/n, где qe —уравновешивающая способность, связанная с концентрацией с, а k, К и п — соответствующие параметры. Если обрабатывается комплексная смесь растворенных веществ, то эти простые модели могут оказаться непригодными.[ ...]
Поверхностно-активные вещества (ПАВ) и красители — типичные загрязнители сточных вод. Активные триазолоновые красители полностью сорбируются из воды на угле КАД-молотый, его максимальная статическая емкость достигает 24,5—54 мг/г [84]. Сорбция из смеси красителей различного типа значительно хуже. Сложность очистки сточных вод текстильных предприятий обусловлена наличием в них разнотипных красителей, присадок и закрепителей с различными сорбционными характеристиками. Так, у девяти изученных красителей и шести присадок коэффициенты в уравнении Фрейндлиха (Г = КС1/п) составляли: у красителей /С = 0,042—65 и л = 0,17—1,4; у присадок К — = 2,5• 10—6 — 180 и л = 0,19—4,2 [85]. Аналогичные результаты получены ВНИИ ВОДГЕО при сорбционной очистке стоков ситценабивных фабрик без предварительной обработки воды. При Ду = 0,5—5 г/дм3 ряд красителей в статических условиях сорбируется на 40—50%, в то время как прямые и сернистые — лишь на 10—20%. Однако иные методы обесцвечивания этих стоков еще менее эффективны. Оптические отбеливатели сорбируются на АУ на 50—60%.[ ...]