Жидкостная хроматография представляет собой метод разделения компонентов смеси, основанный на распределении веществ между двумя несмешивающимися фазами: неподвижной и подвижной жидкой фазой, которая проходит через слой неподвижной фазы. Различают два вида жидкостной хроматографии: твердо-жидкостная и жидко-жидкостная. Твердо-жидкостная хроматография является адсорбционной хроматографией. Наполнитель колонки и условия разделения выбирают экспериментально. Чаще всего в качестве адсорбента (наполнителей) используют силикагель, уголь и оксид алюминия. Адсорбент, покрытый тонкой пленкой диоксида кремния (например, гюрасил), обеспечивает лучшее разделение, чем обычный силикагель. Жидко-жидкостная хроматография является распределительной хроматографией. Жидкость, используемую в качестве неподвижной фазы, наносят на инертный носитель и через слой полученного наполнителя пропускают поток жидкости — подвижной фазы, которая не должна смешиваться с неподвижной фазой [209. 210, 211].[ ...]
Газо-жидкостная хроматография также является распространенным и эффективным методом определения остаточных количеств пестицидов в воде (47, 79). Непрерывное усовершенствование аппаратуры и приемов подготовки проб для анализа позволяет проводить газо-хроматографическое определение пестицидов с большой чувствительностью и точностью. Широкое применение для определения галогенсодержащих соединений получил электронно-захватный детектор [80, 81]. При работе с этим детектором предъявляются повышенные требования к способам очистки экстрактов, к чистоте используемых химических реактивов, посуды [82, 83]. Было отмечено, что посторонние пики реже появляются на хроматограммах при извлечении пестицидов из водных проб прямым экстракционным способом [84] по сравнению с угольно-адсорбционным способом извлечения [85—88].[ ...]
Впервые жидкостную хроматографию в экологических целях использовали Винтерштейн и Шен в 1934 г. при исследовании сложных смесей канцерогенных продуктов, содержащихся в каменноугольной смоле [1]. Эти ученые применили вариант метода адсорбционной хроматографии, разработанный Цветом (см. главу I) для анализа хлорофилла. Некоторые ПАУ были успешно выделены на оксиде алюминия, и на протяжении последующих 30 лет именно ЖХ использовали для извлечения ПАУ из смол, аэрозолей, автомобильных выхлопов и других источников, представляющих интерес для ученых, изучающих канцерогенные вещества. Позднее ЖХ успешно применяли для разделения других потенциальных канцерогенов, таких как азаарены (см. выше), первичные ароматические амины и гетероциклические имины.[ ...]
Разделение веществ в жидкостной хроматографии основано на различии адсорбционных свойств компонентов смеси, растворенных в жидкой фазе. Неподвижная фаза (адсорбент в колонке) должна быть инертна по отношению к подвижной фазе (растворителю) и разделяемым компонентам.[ ...]
Киселев А. В., Яшин Я. И. Адсорбционная газовая и жидкостная хроматография.— М.: Химия, 1979. — 284 с.[ ...]
На ранней стадии развития газовой хроматографии (50—60-е годы) использовались лишь насадочные колонки, представляющие собой стальные или стеклянные трубки длиной 1—5 м и внутренним диаметром 3—4 мм. Колонки заполнялись адсорбентом (адсорбционный вариант газовой хроматографии) — активным углем, силикагелем, оксидом алюминия и др. или сорбентом (газо-жидкостный вариант газовой хроматографии). Сорбент состоял из твердого диатомитового носителя (похожего на размолотый кирпич), на который наносилась в количестве 5—20% НЖФ (вязкая органическая жидкость). Эффективность таких колонок составляла несколько тысяч т.т., и они не позволяли добиться полного разделения многокомпонентных смесей органических соединений, какими являются смеси веществ, загрязняющих воздух, воду и почву.[ ...]
Метод высокопроизводительной колоночной хроматографии применим ко всем упомянутым фазовым сочетаниям (жидкостножидкостная, жидкостно-адсорбционная, ионообменная и гель-хроматография) (см. [71] и [246а]).[ ...]
По природе используемого сорбента газовая хроматография делится на: 1) газо-адсорбционную, 2) газо-жидкостную и 3) капиллярную.[ ...]
Процесс применяют в ряде вариантов (ионообменная хроматография, жидкостно-жидкостная, жидкостно-адсорбционная, гель-хроматография) . В качестве детекторов используют дифференциальные рефрактометры, кондуктометрические датчики, фотометры, адсорбционные калориметры и др. В жидкостной хроматографии используют современные серийные приборы, не уступающие по возможностям и даже превосходящие приборы, которыми оснащена газовая хроматография. Это наглядно видно на примере разделения аммиака и смеси метиламинов методом ионообменной хроматографии [21]. Анализ пробы, содержащей 300—600 мг/дм3 аммиака, 140—150 мг/дм3 метиламина и по 10—50 мг/дм3 диметил- и триметиламинов, занимает 16 мин (объем пробы, вводимой в прибор, 0,05 см3).[ ...]
| Хроматографические колонки, применяемые в адсорбционно-жидкостной хроматографии | 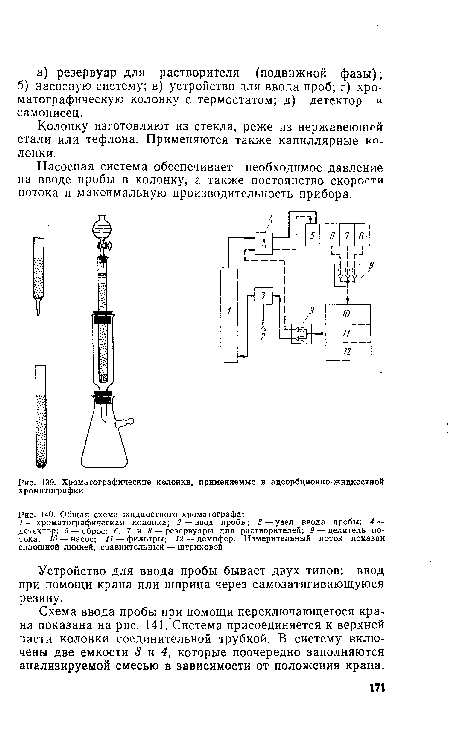 |
Если в случае прямого ГХ— или ВЭЖХ-анализа проб, полученных жидкостно-жидкостной экстракцией, наблюдается низкая эффективность разделения компонентов или нежелательное нарушение профиля хроматограммы, требуется дополнительная очистка образца. Наиболее широко используемый метод очистки — адсорбционная колоночная хроматография на оксиде алюминия, флоризиле и/или силикагеле, применяемый, например, для фракционирования пестицидов и ПАУ. В общем, адсорбция полезна для отделения анализируемых веществ с хорошо известными и узкими диапазонами полярности от мешающих компонентов различной полярности. Некоторые недостатки адсорбционной очистки связаны с изменчивостью активности адсорбентов и необходимостью использования больших количеств растворителей высокой чистоты, которые затем должны быть удалены с тем, чтобы добиться обогащения анализируемых соединений [ I ].[ ...]
Здесь имеются два подхода: метод элюотропных рядов, который получил законченное развитие в корреляционной теории адсорбционной жидкостной хроматографии и молекулярная теория адсорбции.[ ...]
Для идентификации и количественного определения органических соединений со сходной структурой хроматографические методы часто оказываются незаменимыми.[ ...]
Общей характеристикой хроматографических методов является селективное разделение смесей веществ между неподвижной и подвижной фазами. В газовой хроматографии роль подвижной фазы выполняет газ-носитель, в который вводят испаряемую пробу и вместе с ней проводят над неподвижной фазой. В качестве неподвижной фазы может служить сухой адсорбент (газо-адсорбционная хроматография) или жидкость, нанесенная на инертный носитель (газо-жидкостная хроматография).[ ...]
В газо-хроматографнческих методах анализируемая проба вводится в виде паров в газ-носитель и вместе с ним проходит через колонку для разделения над твердой адсорбирующей поверхностью (газо-адсорбционная хроматография) или над твердой поверхностью с нанесенной на нее нелетучей жидкостью (газо-жидкостная хроматография). При этом отдельные компоненты смеси в соответствии с их различными коэффициентами распределения между неподвижной и подвижной фазами проходят с различной скоростью через колонку, выходят из колонки в составе различных фракций в смеси с газом-носителем и количественно определяются с помощью соответствующего детектора. Следует подчеркнуть селективность метода (в данном случае несколько сотен тысяч теоретических тарелок) и его высокую чувствительность (нижний предел обнаруживания до 1 ■ 10—13 г).[ ...]
К хроматографическим методам разделения и концентрирования относят процессы распределения веществ между подвижной (жидкой или газовой) и неподвижной (твердой или жидкой) фазами. На применении хроматографии в настоящее время базируется большинство современных методов пробоподготовки при анализе суперэкотоксикантов, особенно в случае следовых количеств [5). Среди них наибольшее распространение получила жидкостная хроматография, в основе которой лежит распределение вещества между неподвижной твердой и подвижной жидкой фазами. Существуют различные виды взаимодействий между разделяемыми соединениями и твердой фазой: адсорбция, ионный обмен, гель-фильтрация и др. В наиболее часто применяемой адсорбционной хроматографии разделение составных частей пробы достигается благодаря различной полярности органических веществ. При этом компоненты пробы адсорбируются на поверхности твердой фазы и удерживаются на ней благодаря образованию нековалентных (например, водородных или гидрофобных) связей или за счет сил Ван-дер-Ваальса. В ионообменной хроматографии из подвижной фазы на твердом ионообменнике сорбируются противоположно заряженные ионы (органические и неорганические), тогда как в гель-хроматографии в качестве твердой фазы применяются гели, содержащие поры определенного диаметра. Молекулы, размер которых больше диаметра пор, не могут проникнуть внутрь геля. Поэтому при прохождении подвижной фазы в первую очередь элюируются соединения с молекулами большого размера.[ ...]
Оксиды углерода и большая часть других постоянных газов атмосферы отличаются малой полярностью и высокой инертностью, что затрудняет применение химических методов для их анализа. В связи с этим для анализа постоянных газов особенно важное значение получила газовая хроматография. Почти не используют для подобных анализов и вариант газо-жидкостной хроматографии — капиллярную хроматографию. Причины заключаются в том, что постоянные газы малорастворимы при обычных температурах и давлениях во всех жидкостях, которые используют в настоящее время в качестве неподвижных фаз для газо-жидкостной хроматографии ,[173]. Однако в последнее время повысился интерес к низкотемпературной газовой хроматографии. Газовые хроматографы, в которых разделительные колонки могут быть охлаждены до температуры :(—50) — (—100°С) [63, 174], возможно позволят применить для анализа постоянных газов и газо-жидкостную хроматографию.[ ...]
Для спектрофотометрического анализа вещество вымывают соответствующим растворителем, добавляют, если нужно, окрашивающий реагент и проводят измерение. Ошибки определения вызываются главным образом загрязнением исследуемых ■Проб, растворителя и адсорбента, неполным извлечением анализируемых соединений. Так как примеси поглощают в основном в УФ-области спектра, определение исследуемых веществ лучше проводить в видимой части спектра. Пределы обнаружения исследуемых соединений с применением оптических методов детектирования зависят от ряда факторов, в том числе и от природы соединений, и изменяются в широких пределах. Так, при измерении флуоресценции минимально определяемые количества веществ составляют 0,05—10 мкг. Анализ сложной смеси может потребовать повторного разделения. В этом случае первой ступенью является грубое фракционирование соединений пробы с различными функциональными группами методом адсорбционной хроматографии в тонком слое. Затем разделенные зоны вещества, соскабливают, удаляют с адсорбента и разделяют методами газовой или высокоэффективной жидкостной хроматографии.[ ...]