Обменная емкость глинистых минералов Е определялась по катиону Ва2+. Исходя из полученных значений Е, вычислялось количество полимера Э, которое может быть адсорбировано на поверхности глинистых частиц при условии, что в адсорбции принимают участие все активные группы полимера.[ ...]
Адсорбция активированным углем эффективна для большинства органических соединений и используется для очистки бытовых стоков, жидких отходов перегонки нефти, фенолов, ксилола, ароматических углеводородов. Биогенные элементы — азот и фосфор, вызывающие гибель водоемов, удаляют из сточных вод: азот — физико-химическим методом (ионным обменом) в сочетании с биологическим методом, а фосфор — химическим осаЖДе" нием с применением солей железа и алюминия или извести.[ ...]
Обмен ионов происходит таким образом, что органические катионы аналогично катионам металлов вступают в реакции обмена, причем этот эффект (следовательно, ионные свойства органических катионов) зависит от pH среды. Адсорбция на поверхности глинистых минералов обусловливается и другими факторами, например водородной связью, ионными диполями, физико-химическими свойствами обменивающихся молекул, а также молекулярной массой, наличием специфических функциональных групп, конфигурацией и размерами молекул. Кроме того, способность к обмену в значительной мере зависит от отношения обменивающейся молекулы к воде и заполнения активных центров минерала молекулами воды. Последнее обстоятельство может играть решающую роль в процессе обмена.[ ...]
Адсорбция находит применение для глубокой очистки вод замкнутого водопотребления и доочистки сточных вод от органических веществ. Ионный обмен является одним из основных способов умягчения, опреснения и обессоливания вод.[ ...]
Обменная адсорбция имеет ряд особенностей. Во первых, она специфична, т.е. к обмену способны только определенные ионы, и на нее сильно влияет природа как твердой фазы, так и адсорбированного иона. Во вторых, обменная адсорбция не всегда обратима. В третьих, она протекает медленнее, чем адсорбция неэлектролитов при обычной сорбции, особенно в тех случаях, когда в обмене участвуют ионы, находящиеся в глубине адсорбента. И наконец, при обменной адсорбции может происходить изменение pH среды. Если адсорбент отдает водородный ион в обмен на другой катион, то pH среды уменьшается, и она подкисляется. Такой адсорбент называется кислотным. Если адсорбент отдает в раствор гидроксильный ион в обмен на анион, то раствор подщелачивается, а адсорбент называют основным.[ ...]
В обмен на эти ионы растение способно получить соответствующее количество других ионов извне. Наличие участков с положительными и отрицательными зарядами на поверхности корневых волосков объясняется мозаичностью вещества протоплазмы и амфо-дитоидной природой ее белковых веществ. Этим и обусловливается возможность одновременной адсорбции и катионов, и анионов.[ ...]
При адсорбции из растворов вместе с молекулами адсорбируются и ионы. Адсорбция ионов называется полярной адсорбцией. Например, основной краситель, т. е. краситель, у которого окрашенный ион заряжен положительно, адсорбируется на электроотрицательных адсорбентах, и наоборот. Здесь имеет место обмен ионами между адсорбентом и красителем.[ ...]
Ионный обмен основан на частном случае адсорбции (Аотош, 1999), на так называемой обменной адсорбции. Последнее имеет место в тех случаях, когда на поверхности адсорбента, приводимой в контакт с раствором электролита, уже адсорбирован другой электролит, что приводит к обмену ионов между поверхностным слоем адсорбента и жидкости. При этом адсорбент, поглощая определенное количество каких-либо ионов, одновременно выделяет в раствор эквивалентное количество других ионов того же знака, вытесненных с поверхности.[ ...]
Ионный обмен имеет некоторое сходство с адсорбцией: в обоих случаях твердое тело поглощает растворенное вещество. Принципиальное различие между ними состоит в том, что ионит взамен поглощенных ионов отдает в раствор эквивалентное количество противоионов с таким же знаком заряда, а адсорбент только поглощает растворенное вещество, не отдавая в раствор другого. Несмотря на четкое различие, на практике нередко трудно провести границу между названными процессами, поскольку ионный обмен почти всегда сопровождается адсорбцией. .[ ...]
Гипотеза обменной адсорбции легко объясняет избыточное поглощение одного иона из находящейся в растворе соли (рис. 6).[ ...]
Механизм адсорбции газа твердой поверхностью в основном сходен с механизмом жидкостной абсорбции, так как молекулы газа диффундируют через двойной слой на поверхности раздела: твердое вещество — газ. Однако молекулы удерживаются на твердой поверхности, их концентрация .растет, градиент концентраций, являющейся движущей силой процесса диффузии, умень шается и преобладающим процессом становится равновесный обмен молекул.[ ...]
Вторичная адсорбция также подразделяется на обменную и вандерваальсову. Последняя приводит к удержанию вблизи всей поверхности адсорбента как ионов, так и молекул, вследствие чего формируется слой ориентированных дипольных молекул растворителя, а также недиссоциированных молекул, что служит причиной дополнительного скачка потенциала на поверхности раздела фаз.[ ...]
Вторичная обменная адсорбция имеет большое значение для радиохимического разделения и выделения элементов, так как в ней принимают участие все ионы, присутствующие в растворе со знаком заряда, противоположным знаку заряда внутренней обкладки двойного электрического слоя. К вторичной обменной адсорбции применим закон действующих масс, и она зависит от ряда факторов: заряда поверхности осадка, работы адсорбции, размера поверхности осадка [33, с. 62—65].[ ...]
Первичная адсорбция, при которой адсорбируемые ионы входят в состав поверхности осадка, подразделяется на первичную, потенциа-лобразующую и первичную обменную адсорбцию. В потенциалобра-зующей адсорбции принимают участие только те ионы, которые могут входить в кристаллическую решетку осадка, т. е. одноименные или изоморфные ионы. Для радионуклидов, Находящихся в крайне разбавленном состоянии, этот вид адсорбции играет незначительную роль, поскольку радионуклиды не могут обеспечить создания достаточного избытка одного из ионов на поверхности кристаллов, обусловливающих появление на поверхности заряда и скачки потенциала. Избыток того или иного иона микрокомпонента на поверхности наблюдается как в силу неодинакового средства собственных катионов и анионов к поверхности кристалла, так и из-за избытка одного из ионов в растворе. Потенциалобразующая адсорбция косвенно имеет большое значение для адсорбции радионуклидов, поскольку ее величина определяет общую емкость по отношению к вторичной обменной адсорбции.[ ...]
Вторичная обменная адсорбция происходит во внешней обкладке двойного электрического слоя, возникающего на границе кри-сталл-раствор. На адсорбцию микроколичества радионуклида в данном случае оказывают конкурентное влияние все ионы, присутствующие в растворе и имеющие знак заряда, противоположный заряду поверхности. Величина вторичной обменной адсорбции ионов зависит от заряда и величины поверхности кристаллического тела, от величины работы адсорбции, валентности ионов, ионной силы раствора, концентрации потенциапобразующих ионов в растворе.[ ...]
| Схема обменного поглощения ионов протоплазмой и их передвижения в ней путем адсорбции-десорбции (по Бруксу). | 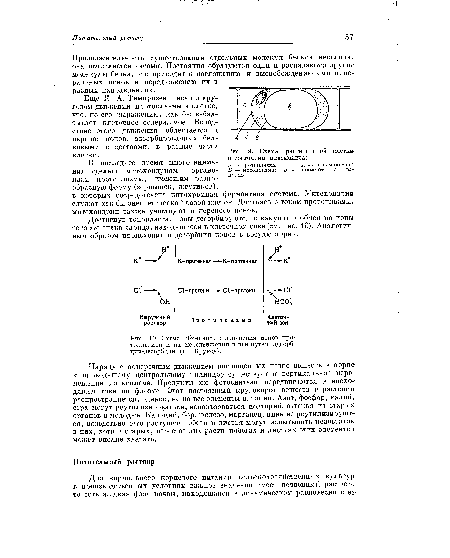 |
При вторичной адсорбции ионы не входят в состав кристаллической решетки и остаются в прилегающем к кристаллу тонком слое раствора. Этот вид адсорбции подразделяют на вторичную обменную и ван-дер-ваальсову адсорбцию.[ ...]
Адсорбционный обмен ионами между деятельной поверхностью корневой системы и почвенным раствором до некоторой степени объясняет механизм процессов поступления и перемещения ионов при корневом питании. Обменная адсорбция протекает с очень высокой скоростью. Неэквивалентное поглощение ионов электролита растением, как и движение их против градиента концентрации, тоже легче разъяснить с позиции ионного обмена. Между тем как для диффузно-осмотического пути непонятно поступление солей из раствора с меньшей концентрацией (почва) в среду с более высокой концентрацией их (клеточный сок растения).[ ...]
Растворение солей, адсорбция и ионный обмен имеют место и при проникновении воды в глубь почвы. Длительность взаимодействия воды с почвой, контакт с подстилающими породами и фильтрация через грунты обусловливают особенности состава, присущие подземным водам.[ ...]
В некоторых случаях адсорбция происходит в результате ион- ного обмена. Предполагается, что на частицах глинистых минералов возможен как катионный, так и анионный обмен.[ ...]
Таким образом, гипотеза обменной адсорбции вполне удовлетворительно объясняет первый этап усвоения веществ растением из окружающего его раствора.[ ...]
В случае ван-дер-ваальсовой адсорбции происходит одновременно адсорбция по всей поверхности противоположно заряженных ионов в эквивалентных количествах. В этом виде адсорбции также наблюдается обмен. Обмениваются электролит в форме молекул или ионного ассоциата с молекулами адсорбированной воды. Для микроколичеств радионуклидов обычно считают, что этот вид адсорбции играет вторичную роль.[ ...]
Эти методы включают: ионный обмен, адсорбцию на инертных материалах и природных сорбентах, коагуляцию с добавлением различных коагулянтов, экстракцию, пенную сепарацию, химическое осаждение в виде нерастворимых соединений, деструктивное разрушение.[ ...]
Нужны новые методы очистки: адсорбция, дистилляция, электродиализ, удаление пены, эвтектическое замораживание, ионный обмен, обратный осмос. Опыты показали, что при удлинении -продолжительности третичной очистки до 24 ч БПК6 сточных вод снижается на 90%. При комбинации вторичной и третичной очистки можно снизить загрязненность сточных вод органическими веществами на 98—99%.[ ...]
Физико-химическое, коллоидальное, обменное поглощение. Физико-химической поглотительной способностью почв К. К- Гедройц назвал явление обмена катионов, содержащихся на поверхности твердой части почвы, на эквивалентное количество катионов, находящихся в почвенном растворе. Этот вид поглощения теперь чаще называют коллоидальным, или обменным поглощением, а также обменной адсорбцией.[ ...]
Ионы могут поглощаться не только в обмен на Н и НС03, но и в результате обменной адсорбции на ионы других корневых выделений, как органических, так и минеральных. Значительной может быть роль органических кислот (лимонной, яблочной, щавелевой и др.), наличие которых в выделениях корне давно доказано.[ ...]
Очистка сточных вод — химическими [2; 21—23; 25; 29] и биологическими методами [0-47], ионным обменом [2], адсорбцией на активном 5 гле [27]. Предложены автоматические методы [30; 31].[ ...]
Резервуарный фонд серы обширен в почве и отложениях, меньший - атмосфере. Основную роль в обменном фонде серы играют особые микроорганизмы, каждый вид которых выполняет определенную реакцию окисления и восстановления; в результате микробной регенерации серы из глубоководных отложений к поверхности перемещается сероводород. В глобальном масштабе в регуляции круговорота серы участвуют геохимические и метеорологические процессы (эрозия, осадкообразование, выщелачивание, дождь, адсорбция и т.д.), биологические процессы (продукция биомассы и ее разложение), взаимосвязь воздуха, воды и почвы. Сульфат аналогично нитрату и фосфату - основная доступная форма серы, которая восстанавливается авто-трофами и включается в белки (сера входит в состав ряда аминокислот).[ ...]
При ионообменной обработке сточных вод, содержа-днх органические примеси, наряду с ионным обменом протекают :роцессы хемосорбции и физической адсорбции органических веществ ионитами [165, с. 40; 439].[ ...]
Из рис. 7 видно, что при фильтрации раствора,некаля через Анекс—Л происходит главным образом обмен ионов и только в последней фазе наступает адсорбция некаля.[ ...]
Равновесие С 02 в атмосфере является важным предметом химии окружающей среды. Процессы образования С02 при обмене веществ, его адсорбция водами морей и океанов, поглощение при фотосинтезе, равновесие между этими процессами — все эти вопросы нуждаются в более полных и точных исследованиях. Период, в течение которого мы сможем использовать ископаемые топлива после 2000 г., зависит от ответа на эти вопросы.[ ...]
По их данным, стабилизирующим электролитом золя А1(ОН)3 является соединение А1203-НС1, которое, взаимодействуя с коагулирующим электролитом (например, Na2S04), образует хорошо адсорбирующуюся соль — в данном случае ок-сисульфат A1203-H2S04. Степень адсорбции определяется концентрацией и растворимостью соли и меняется с изменением pH. Уменьшение содержания S04 -hohob в осадке при понижении pH объясняется увеличением растворимости оксисульфата, а при повышении pH — малым содержанием в интермицеллярной жидкости А1203-НС1. Область существования малорастворимых солей соответствует значениям pH среды 3—6,5.[ ...]
Как видно из рисунка, речь идет не об осмотическом поглощении (всасывании) корневым волоском питательной соли, а об адсорбционном обмене между ним и внешним раствором, или жидкой фазой в более широком смысле, катионами и анионами (показано на примере калия). Это не следует понимать так, что осмос вообще не имеет значения для поступления питательных веществ в растения. Этот путь сохраняет свою роль при поглощении недиссоци-ированных молекул, но в случае обмена ионами (а он преобладает) адсорбция объясняет явление гораздо лучше и с точки зрения скорости процесса, и в отношении движения от меньшей концентрации раствора к более высокой, и применительно к избирательному (неэквивалентному) удалению из раствора одного из ионов любой соли.[ ...]
Для черноземных почв значение у колеблется от 0,7 до 2, для подзолистых — от 0,03 до 0,34. При взаимодействии воды с почвой, кроме растворения солей, наблюдаются явления адсорбции и ионного обмена. Академик К. К. Гедройц разработал учение о почвенном поглощающем комплексе, состоящем из органических и минеральных соединений. Этот комплекс служит важным. источником питания растений, поставляя в почвенный раствор необходимые для растений катионы в обмен на ионы водорода, содержащиеся в кислом соке, который выделяется корнями растений.[ ...]
В присутствии же нескольких солей неизбежно происходит своеобразная конкуренция между ионами одного знака заряда за поступление в растение, что мешает преимущественному обменному поглощению корнями одного из них. Это явление получило название антагонизма ионов. Оно проявляется в том, что катионы разных элементов мешают друг другу при их адсорбции на деятельной поверхности корней, причем здесь сказывается значение их валентности: одновалентные катионы менее конкурентноспособны, чем двухвалентные.[ ...]
Многие пестицидные препараты могут быть эффективно удалены из воды с помощью природных сорбентов. Изучена [42] сорбция различных эфиров тиофосфорной кислоты в зависимости от замещения природного обменного комплекса монтмориллонита на другие катионы.[ ...]
При производстве инсектицидов мышьяк утилизируют целиком и в сточные воды он не поступает [45]. Из сточных вод других производств мышьяк извлекают в основном химическими методами [46—53]. Используются и физико-химические методы — адсорбция на активном угле [0-55], ионным обменом [54] и др. Двойным биофильтрованием мышьяк извлекается из сточных вод полностью [55].[ ...]
Гальваношламы отличаются удельной поверхностью, которая зависит от способа образования гидроксидов, сульфидов и карбонатов металлов (А1, Ре, Сг, Си, Zn и др.). Огромная удельная поверхность придает гальваношламам большую поверхностную активность, способность к адсорбции и обменным реакциям [55].[ ...]
Обобщая вышеизложенные сведения о трансформации буровых реагентов, нефтешламов, нефти и нефтепродуктов в почве и воде, следует еще раз подчеркнуть, что это сложный процесс, на который оказывают влияние особенности гранулометрического состава почв, содержание органического вещества и обменных катионов, а также химический состав нефти и ее свойства. Большое значение также имеет характер их распространения в среде, включая процессы испарения и конденсации, диффузии, адсорбции и десорбции, биодеградации под воздействием микроорганизмов и различные реакции абиотического расщепления. При этом важно также учитывать физико-химические характеристики: растворимость углеводородов, точку кипения, давление паров и др., а также условия, при которых протекает биологическое окисление загрязнителей, адсорбированных частичками почвы, роль органических и неорганических почвенных коллоидов и т. д. Необходимо принимать во внимание и характер миграционных процессов, которые, с одной стороны, приводят к широкому распространению загрязнения за пределы исходного района за счет горизонтальной миграции низко- и среднемолекулярных углеводородов, а с другой - приводят к концентрации в зоне загрязнения высокомолекулярных компонентов нефти и буровых реагентов в верхних слоях почвы.[ ...]
Ниже рассмотрен механизм действия газообразных загрязнений. В зависимости от доз, получаемых растениями, диоксид серы может оказывать как положительное, так и отрицательное действие. При малых концентрациях он является дополнительным источником питания, при высоких — резко ухудшается обмен веществ и возможна быстрая гибель растений. Это обусловлено преимущественно -изменением количества углеводов — при малых дозах диоксида серы оно увеличивается, а при повышенной концентрации диоксида — уменьшается. Устойчивость растений к диоксиду серы определяется двумя факторами — активностью устьиц листа и скоростью адсорбции диоксида серы на поверхности, а также способностью переводить токсичный сульфит в неактивный сульфат (как это наблюдается у бобовых).[ ...]
Так как с помощью физико-химических процессов невозможно удалить столько органических веществ, сколько удаляется в результате биологических процессов, то их используют в основном для обработки стабилизированных биологической очисткой фильтрующихся вод. Ни один из испытанных физико-химических способов очистки: химическая коагуляция и осаждение, адсорбция активным углем, обратный осмос, адсорбция на полимерах, химическое окисление (включая озонолиз), выпаривание и облучение — не оказался полностью эффективным. Например, озонолиз, адсорбция на активном угле, катионный и анионный обмен и обратный осмос понижали концентрацию органического углерода на 48, 86, 53, 82—85 и 91—96% соответственно. Напротив, химическая коагуляция и осаждение в присутствии извести, квасцов, хлорида железа(III), сульфата железа(II) и полимеров удаляет малую часть органических веществ, но большую— тяжелых металлов и взвешенных частиц [287].[ ...]
Как было ¡показано выше, .при неизменном значении pH адсорбционная способность глинистых минералов снижается в последовательности монтмориллонит- -иллит->-каолинит. В почвах с нейтральной (pH 7) или щелочной (pH 7—10) реакцией между частицами почвы и гербицидом действуют только слабые Ван-дер-Ваальсовы силы. При этих условиях возможна только молекулярная адсорбция. В кислой же среде начинают проявляться силы электростатического взаимодействия, и вследствие этого в кислых почвах на так называемых Н-глинных минералах адсорбция идет гораздо сильнее. Величина адсорбции зависит от количества обменных ионов водорода (или одновалентных катионов) в почве. В нейтральной и особенно в щелочной среде (pH выше 7), например в кальциевых глинных минералах, гербициды адсорбируются гораздо слабее. Добавление в такие почвы кислых минеральных удобрений приводит к усилению, а извести — к ослаблению их адсорбционной способности.[ ...]
Поступление ионов №+ и К+ в природные воды обусловлено выщелачиванием их при выветривании коренных пород, содержащих алюмосиликаты ■натрия (оливина, альбита, нефелина и др.), и кислых пород вулканического происхождения, содержащих калий (ортоклаза, мусковита, плагиоклаза, биотита и др.). Ионы Ма+ появляются и в результате растворения ЫаС1, присутствующего в осадочных породах в виде огромных залежей, а также вследствие обменной адсорбции из растворов Са2+ в породах; взамен поглощенных ионов кальция в воде появляются эквивалентные количества Ыа+ . В породах вулканического происхождения содержание натрия и калия примерно одинаковое . Большое значение отношения №+ : К+ в воде объясняется лучшей сорбцией К+ поглощающим комплексом почв и пород, а также тем, что он извлекается растениями в больших количествах, чем натрий[ ...]
Атмосферные осадки являются маломинерализованными растворами. На некоторых станциях их среднегодовая минерализация не превышает 6—8 мг/л. Работа с такими растворами требует большой аккуратности при анализе. Определенные требования к анализу связаны также и с тем, что с течением времени даже в герметически закрытых сосудах происходит изменение солевого, газового и ингредиентного состава. Главной причиной изменения компонентного состава является как выщелачивание химических элементов из посуды, так и ионный обмен или адсорбция растворенных веществ на стенках сосудов, особенно стеклянных.[ ...]