Гипосульфит и бикарбонат натрия стерилизуют отдельно, растворив в небольшом количестве воды, и добавляют в стерильный раствор остальные соли после охлаждения.[ ...]
Растворимость бикарбоната кальция при углекислотном равновесии пластовой воды с атмосферным воздухом значительно ниже, чем при пластовых (либо промежуточных) условиях. Поэтому пластовые воды при очистке их в сооружениях открытого типа почти всегда имеют некоторое пересыщение бикарбонатом кальция. Величина пересыщения, равная разности между общим и равновесным его содержанием, показывает количество осадка, которое может образовываться при разложении избытка бикарбоната. Однако равновесное содержание бикарбоната кальция, соответствующее какому-либо химическому составу воды, не может быть найдено расчетом, который применим только для простых смесей электролитов, не имеющих общих с бикарбонатом кальция ионов [2—4]. Поэтому соответствующая величина находилась экспериментально.[ ...]
Проведены опыты с раствором бикарбоната кальция, приготовленным на бидистилляте, в котором практически полностью отсутствуют примеси железа. В этом случае никакого изменения процесса кристаллизации после омагничивания не наблюдалось. Развивая это направление, В. И. Катков и Е. Ф. Тебенихин [13, с. 276—283] полагают, что магнитная обработка эффективна только при образовании ферромагнитных агрегатов, которые под действием пондеромоторных сил вызывают перемешивание и ускоряют кристаллизацию из пересыщенного раствора, а также играют роль затравок. В подтверждение они приводят результаты опытов с растворами, в которые вводили суспензии магнетита Ре304 и оксида железа Ре203. При магнитной обработке эти частицы коагулируют. Опыты также показали, что эти частицы могут служить центрами кристаллизации и могут значительно ее ускорять [78].[ ...]
Образующаяся при разложении бикарбоната натрия сода вместе с избыточной содой, введенной вначале в водоумягчитель, тут же в котле гидролизуется водой на едкий натр и углекислоту. Последний с продувочной водой поступает в водоумягчитель, где используется для удаления из умягчаемой воды бикарбонатов кальция и магния. Недостаток метода состоит в том, что накопление большого количества С03 в процессе умягчения приводит к коррозии металла и повышению содержания сухого остатка в котловой воде.[ ...]
Из этого выражения видно, что бикарбонат-ионы существуют в растворе только при наличии свободной углекислоты. Часть свободной углекислоты, находящейся в равновесии с бикарбонатами, называется равновесной. Она как бы связана с бикарбонатами и поэтому не вступает в химические реакции.[ ...]
Обычно установки для удаления бикарбоната железа состоят из специального устройства, обеспечивающего окисление закиси железа кислородом и удаление углекислоты; контактных резервуаров или заполненных песком контактных фильтров, где завершается процесс окисления; осветлительных фильтров для удаления выпавшей гидроокиси (аналогично фильтрам, применяемым для осветления воды).[ ...]
Эфирный раствор (5эф) действием бикарбонатом натрия делится на кислоты ( 5) и фенолы (Я3), которые затем разделяются на группы летучих и нелетучих кислот и летучих (£>2) и нелетучих фенолов (№).[ ...]
В осадок выпадает белый кристаллический бикарбонат аммония. Остающийся в растворе двууглекислый аммоний насыщают газообразным аммиаком [МН4НС03 + ГШ3 = (№Н4)2С08]. Образующийся в растворе карбонат аммония вновь используют для производства бикарбоната аммония. Удобрение содержит около 17% азота. Оно обладает несколько большей стойкостью по сравнению с карбонатом аммония, но все же при хранении, перевозках и внесении не исключены потери аммиака. При разбросном внесении бикарбонат аммония следует заделывать в почву немедленно.[ ...]
При одновременном присутствии в воде гидратов, бикарбонатов и карбонатов раздельное определение щелочности по фенолфталеину (Ф) и метилоранжу (М) позволяет вычислить отдельные компоненты щелочности воды (табл. I—13).[ ...]
Для раздельного определения гидратов, карбонатов и бикарбонатов в воде применяется последовательное титрование с двумя индикаторами- фенолфталеином, дающим переход окраски при рН-8,3 и метилоранжем, менявшим окраску при pH - 4,4.[ ...]
Кроме того, обращает внимание низкое содержание фтора, бикарбонатов кальция и магния, что должно было весьма отрицательно отразиться на вкусовых качествах такой воды, не говоря уже о ее полноценности вообще.[ ...]
Основными загрязнениями являются хлориды, сульфаты, карбонаты, бикарбонаты и в очень небольшой степени никель, «активный хлор» и грубодисперсные примеси.[ ...]
Вероятность образования накипи зависит не только от содержания бикарбоната кальция. На этот процесс оказывает влияние интенсивность упаривания воды в системе, величина потери углекислоты при разбрызгивании воды, наличие в последней органических веществ, стабилизирующих карбонат кальция и препятствующих его выпадению.[ ...]
Оставшаяся в воде углекислота в Ыа-катионитовых фильтрах образует бикарбонат натрия.[ ...]
Следует отметить наличие в подземных водах марганца в виде закиси МпО и бикарбоната Мп(НСОз)г.[ ...]
Вариант 2. Эфирный раствор экстрагируют тремя небольшими порциями раствора бикарбоната натрия, отделяют эфирный слой и экстрагируют его тремя порциями по 30 мл раствора едкого натра. Затем эфирный слой отделяют, высушивают его безводным сульфатом натрия и отгоняют эфир. Полученный остаток состоит из нейтральных соединений, содержавшихся в пробе; его взвешивают.[ ...]
Устранимая или временная (Нвр) и карбонатная (Нк) жесткости обусловлены наличием бикарбонатов (и карбонатов) кальция и магния.[ ...]
Принцип метода. Метод основан на сплавлении свободной двуокиси кремния и силикатов с бикарбонатом калия или натрия в присутствии хлоридов. При этом свободная двуокись кремния переходит в растворимую щелочную соль кремневой кислоты, а крем-некислота силиката сохраняется в составе его молекулы, обогащенной щелочью плавня, и в раствор не переходит. Содержание двуокиси кремния определяют колориметрически по желтому кремнемолибденовому комплексу.[ ...]
Аналогичная ситуация — в содовом производстве, где фильтровая жидкость после выделения бикарбоната аммония содержит 190—200 г/дм3 хлорида аммония, а также некоторые количества бикарбоната натрия и сульфата натрия, примеси которого могли быть в исходном хлориде натрия. В содовом производстве аммиак является важнейшим вспомогательным веществом. Количество хлорида аммония (в расчете на аммиак) составляет около 530 кг/т соды. Весь этот аммиак должен быть выделен из раствора и возвращен в цикл.[ ...]
| ИК-спектры пленок МЦ, сшитой ДМАЭ (/), лимонной кислотой (2) и после обработки последней бикарбонатом натрия (3). | 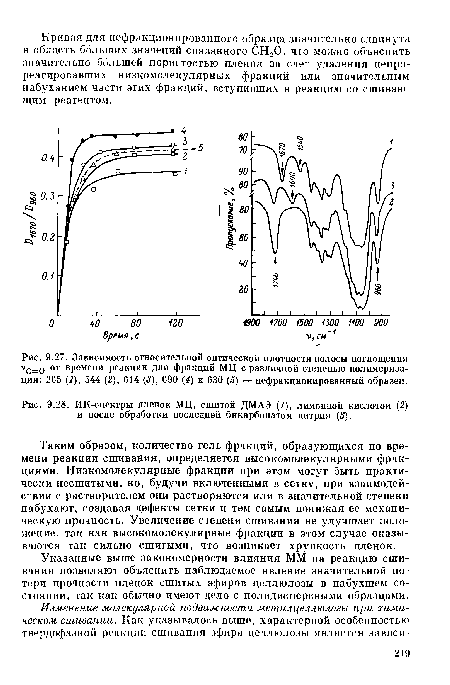 |
В разбавленных водных растворах (<2% полимера) на свету, в присутствии ионов Fe2 и Fe3+, щелочей, карбонатов, бикарбонатов и силикатов, при нагревании выше 25° С и сильном перемешивании , (мешалками, барботажем, перекачиванием насосами) происходит постепенная деструкция полимера. В щелочной среде в водных растворах полимер, гидролизуется до полиметакриловой кислоты.[ ...]
Щелочносульфитная варка проводится в водных растворах смеси моносульфита натрия и различных количеств бикарбоната натрия.[ ...]
Щелочносульфитная варка проводится в водных растворах смеси моносульфита натрия и различных количеств бикарбоната натрия.[ ...]
Жесткость воды зависит преимущественно от наличия в ней растворенных солей кальция и магния. Временная жесткость обусловливается бикарбонатами кальция и магния. Величина постоянной жесткости зависит от содержания главным образом сернокислых солей кальция и магния. Сумма первой и второй составляет общую жесткость.[ ...]
Второй вариант реагентного умягчения заключается в использовании извести совместно с содой. При известковом умягчении после перевода бикарбонатов в карбонаты и их осаждения дальнейшего снижения жесткости не происходит, несмотря на выделение в осадок Мд (ОН) 2. Взамен магниевой жесткости в воде появляется кальциевая некарбонатная жесткость.[ ...]
Ход определения. Анализируемый раствор из каждого поглотительного прибора переносят в колориметрические пробирки, добавляют по 0,2 мл раствора бикарбоната натрия, 0,2 мл раствора йодной кислоты, пробирки встряхивают и помещают на 30 мин в нагретую до 40 °С водяную баню. После охлаждения приливают по 1 мл Нг504 (ё = 1,84), осторожно встряхивают и добавляют одинаковое количество сульфита натрия до обесцвечивания (1—3 капли). Затем приливают по 5 мл раствора хромотроповой кислоты, осторожно встряхивают и нагревают 30 мин на кипящей водяной бане. По охлаждении добавляют 10 мл воды и раствор фотометрируют на фотоэлектроколориметре относительно контрольного раствора в кюветах с толщиной слоя 5 см с желтым светофильтром.[ ...]
При кипячении устраняется, выпадая в виде нерастворимого карбоната кальция, та часть карбонатной жесткости, которая преимущественно состояла из бикарбоната кальция, так как СаС03 менее растворим в отсутствии свободной углекислоты, чем сравнительно легкорастворимый М С03.[ ...]
Причиной отложений является наличие в природной воде различных растворенных солей, а также взвешенных механических примесей: песка, глины, водорослей. Особенно вредно наличие бикарбоната кальция, который при нагревании воды до 50—60° распадается, образуя карбонат кальция, выпадающий в осадок.[ ...]
Умягчение воды, т. е. удаление из нее ионов Са2+ и Л 2+, может осуществляться термическими, реагентными и ионнообменными методами. Термические методы умягчения основаны на переходе бикарбонатов кальция и магния в малорастворимые карбонаты, выпадающие в осадок при кипячении воцы. В случае использования реагентных методов умягчения воды растворимые соли кальция и магния при помощи химических реагентов переводятся в нерастворимые соединения, удаляемые отстаиванием и фильтрованием. Умягчение воды методом ионного обмена основано на обмене ионов Са2+ и А 2+, находящихся в воде, на ионы катионита (№+ или Н+), через который она фильтруется.[ ...]
Более активно, чем другие восстановленные формы, окисляется элементарная сера. Источником углерода для этого организма служит углекислота, так как при оптимальном для него значении pH = 4 бикарбонат не может находиться в растворе. Старки (1925 г.) установил, что ТЫоЬасШиз Шюох1с1апз может переносить высокие концентрации некоторых органических соединений, в то время как другие органические соединения резко подавляют его развитие.[ ...]
Величина ДПкр гидрозоля А1(ОН)3, по данным Рэддика, находится в пределах +15 -=—[-20 мв [15], а согласно экспериментам Кульского и др. [16], она составляет при коагуляции хлоридами +75 мв, сульфатами +25 мв, бикарбонатами +9 мв.[ ...]
Кальциевая селитра физиологически щелочное удобрение. Поэтому ее преимущества перед другими удобрениями проявляются на кислых почвах. Обогащение кальцием поглощающего комплекса, накопление бикарбоната кальция в почвенном растворе содействуют устранению кислой реакции почвы. При многократном внесении азотнокислого кальция в почву физиологическая щелочность его может проявиться достаточно четко. Нейтрализация почвенной кислотности кальцием усиливает жизнедеятельность азотфикси-рующих и других групп бактерий. Д. Н. Прянишников считал кальциевую селитру универсальным удобрением, пригодным для всех почв под всевозможные культуры и прежде всего для почв нечерноземной зоны.[ ...]
Количественное соотношение между этими тремя формами углекислоты при данной температуре зависит от величины pH (рис. При температуре 25°С в пределах pH 7 — 8,4 углекислота находится в форме бикарбонатов; при pH < 4 вся имеющаяся углекислота находится в свободной форме (С02); при pH > 11 ее большая часть связана в СО3-.[ ...]
Гидролиз происходит с достаточной полнотой и скоростью при наличии в воде некоторого резерва щелочности, которая необходима для удаления водорода. Общая щелочность воды представлена главным образом бикарбонатами и в меньшей степени карбонатами и свободной углекислотой. Они и связывают катионы водорода Н+ + НСОз ->■ С02 + Н20.[ ...]
Несжимаемыми называют осадки, у которых пористость (отношение объема пор к объему осадка) не уменьшается при увеличении разности давлений. К таким осадкам относят вещества неорганического происхождения с размерами частиц более 100 мкм (песок, карбонат кальция, бикарбонат натрия и др.). К сжимаемым осадкам относят такие, пористость которых уменьшается, а их гидравлическое сопротивление потоку жидкости возрастает с увеличением разности давлений. К ним относятся осадки гидрооксидов металлов, а также осадки, состоящие из легко деформируемых агрегатов, которые образуются из первичных мелких кристаллов.[ ...]
Своеобразной комбинацией элементов сульфит-бисульфитного и известняково-известкового методов является десульфурация газов угольных ТЭС с использованием в оросительных скрубберах морской воды. Степень удаления Б02 оценивается в 95%. По рассматриваемому методу Германией начато строительство коммерческой установки для Индонезии (Лваку ).[ ...]
А. Исследование кислородного режима и сопряженных с ним факторов (pH, карбонатное равновесие). Кислородный режим является одним из факторов, существенно изменяющихся под влиянием многих токсикантов. Поэтому определять кислород необходимо регулярно и систематически. Наряду с кислородом определяются С02, pH, карбонаты, бикарбонаты и ВПК, причем существенное значение имеют круглосуточные определения содержания растворенных газов, с интервалом через 3—4 часа.[ ...]
Сточные воды многих производств, особенно органического синтеза, содержат амины. Некоторые из них, например триэтиламин, устойчивы к биохимическому окислению. Некоторые исследователи предлагают очищать такие воды и методом озонирования [?9, 80] . Амины окисляются озоном очень легко. Основные продукты окисления - нитраты, бикарбонаты и вода.[ ...]
Мичиган), которая является поставщиком сырья для цехов электролитических покрытий, извлекает никель из осадков, образующихся из сточных вод от установок ее заказчиков. Никель, являющийся дорогостоящим металлом, удаляют из сточных вод, содержащих раствор сернокислого никеля, путем осаждения его бикарбонатом натрия в виде нерастворимого углекислого никеля. Последний осаждают и затем обезвоживают пресс-фильтром до содержания в нем 50 % твердых веществ. Сухой осадок отправляют обратно поставщику в один из четырех региональных центров, где углекислый никель превращают в высококачественный раствор сернокислого никеля [43].[ ...]
Метод Сольвэ состоит в следующем: приготавливают насыщенный раствор поваренной соли, который после осаждения и удаления примесей ионов кальция и магния насыщают аммиаком и получают аммиачный рассол. При последующей карбонизации, т. е. обработке рассола двуокисью углерода, получаемой при термическом разложении известняка, в осадок выпадает бикарбонат натрия, который после фильтрации переводится в карбонат натрия—кальцинированную соду.[ ...]
К 22,7 г О-феняддяхлортиофосфата в 50 мл ацетона прибавляют смесь 24 г этилового эфира тяогляколевой кислоты и 20,2г три-этияамина в 50 мл ацетона при -5-0°С. Массе дают нагреться до комнатной температуры и выдерживают в течение 6 часов при температуре кипения ацетона. Осадок отфильтровывают, фильтрат разбавляют бензолом и промывают несколько раз раствором бикарбоната Яа и водой.[ ...]
Определение суммы свободного и связанного п-нитрофенола. Пробу в количестве 5 мл переводят в колбу, приливают 3 мл 20 % раствора едкого натра и нагревают с обратным холодильником в кипящей водяной бане в течение 15 минут. По охлаждении раствор количественно переводят в колориметрическую пробирку и интенсивность окраски его сравнивают со шкалой стандартов (табл. 227), в пробирки которой вместо бикарбоната натрия прибавляют по 3 мл 20% раствора едкого натра.[ ...]
Прокаленный остаток служит для определения минеральной части растворенных в воде веществ, а по разности сухого и прокаленного остатка оценивается суммарное содержание органических веществ. Прокаленный остаток определяется путем прокаливания сухого остатка при 800°. При этом происходит сначала обугливание, а затем сгорание органических веществ. Одновременно при прокаливании улетучивается оставшаяся влага, частично улетучиваются хлориды, разлагаются бикарбонаты и удаляется С02, а иногда восстанавливаются сульфаты. Поэтому величина прокаленного остатка также может служить лишь весьма приближенной характеристикой общего содержания катионов и анионов в исследуемой воде. По разности сухого и прокаленного остатков столь же прибли женно может быть определено суммарное содержание органических веществ.[ ...]
М. Л. Михельсон [37, с. 3—62] термодинамическими расчетами показал, что магнитные поля могут активировать коллоидные центры кристаллизации. Это влияет на кинетику роста кристаллов солей жесткости на намагниченных частицах магнетита. Представляется возможным обосновать полиэкстремальную зависимость эффекта воздействия от напряженности магнитного поля и экстремальную — от скорости потока (это подтверждено расчетами на ЭЦВМ). Дальнейшие опыты показали, что при одинаковом химическом составе раствора бикарбоната кальция после магнитной обработки кристаллизация на частицах магнетита происходит со значительно большей скоростью, чем на таких же частицах кальцита [24, с. 159—161]. Еще предстоит выяснить и роль заряженных микрочастиц немагнитных примесей.[ ...]
В США работает девять установок по регенерации извести из известкового шлама [12.21]. Опыт работы показал, что эта технология экономически оправдана только при определенных условиях: доля карбоната кальция в шламе, подаваемом в печь, должна быть не менее 90 %, а его влажность не более 30 %. При этом производительность печи по СаО должна быть не менее 50 т/сут. Для уменьшения доли магния в шламе продувку осветлителя обрабатывают углекислым газом, образующимся в процессе обжига. В результате такой обработки осадок гидроксида магния превращается в хорошо растворимый бикарбонат магния и удаляется вместе с жидкой фазой. Уплотненный осадок обезвоживается на вакуум-фильтрах, корзиночных центрифугах или ленточных фильтрах-прессах. Перед подачей в обжиговую печь осадок сушится дымовыми газами. Отработанные дымовые газы подвергаются двухступенчатой очистке. Избыток извести продается.[ ...]
Содержание двуокиси углерода в воде также сильно варьирует, но по своему «поведению» она сильно отличается от кислорода, а ее экологическая роль не так хорошо изучена. Поэтому трудно сделать какие-то обобщения, касающиеся роли ССЬ как лимитирующего фактора. Хотя в воздухе содержание двуокиси углерода невелико, она прекрасно растворяется в воде; кроме того, в воду поступает двуокись углерода, освобождающаяся при дыхании и разложении, а также из почвы или подземных источников. Поэтому «минимальный предел» содержания С02 не имеет такого значения, как в случае Ог- Кроме того, в отличие от кислорода двуокись углерода реагирует с водой, образуя Н2СО3, которая в свою очередь вступает в реакцию с известью, образуя карбонаты (—СОз) и бикарбонаты (—НСОз). А, основным резервуаром СОг в биосфере является карбонатная система океанов. Эти соединения служат не только источником питательных веществ, но и буфером, поддерживающим концентрацию водородных ионов в водных средах на уровне, близком к нейтральному значению. Небольшое повышение содержания С02 в воде Ьовышает интенсивность фотооинтеза и стимулирует процессы развития многих организмов. Высокие концентрации СО2 определенно могут быть лимитирующим фактором для животных, особенно потому, что высокое содержание двуокиси углерода обычно связано с низким содержанием кислорода. Рыбы весьма чувствительны к повышению концентрации СОг: при слишком высоком содержании свободного СОг в воде многие рыбы погибают.[ ...]