В большинстве озер сульфатный ион (по концентрации) занимает второе или третье место, среди растворенных анионов. Сульфаты попадают в озера по большей части с дождями, а также в результате растворения донных пород. Этот ион используется в питательных целях как автотрофными, так и гетеротрофными серобактериями. Он идет на образование аминокислот и выделяется аэробными и анаэробными бактериями соответственно в окисленной форме или в виде ШЭ. Выделение в ходе анаэробного разложения сероуглерода в слое гиполимниона и уменьшение в последнем концентрации растворенного кислорода представляют собой процессы, ответственные за общее ухудшение качества воды. Сероуглерод в растворенном состоянии ведет себя как слабая кислота. Уровень его концентрации в воде отчасти регулируется растворимостью сернистого железа. На рис. 6.9 представлены кривые, отражающие взаимосвязь между концентрациями ионов Ре2+ и молекул Нг5 при различных значениях pH.[ ...]
В последнее время высказывается мнение, что основным каналом поступления серы в озера являются так называемые кислотные дожди (см., например, [561]). Возможно первым водоемом, оказавшимся подкисленным (хотя и не диагностированным должным образом) было озеро в Новой Шотландии [83, 193]. Совсем недавно в скандинавских и североамериканских озерах (особенно в районе Адирондека штата Нью-Йорк) было обнаружено значительное снижение pH в результате кислотных осадков. Во многих озерах Скандинавских стран pH настолько снизилось, что рыбы оказались не в состоянии существовать в такой среде. Однако следует отметить, что даже в одном и том же географическом районе влияние кислотных дождей на существующие там озера неодинаково и различия обусловлены прежде всего естественной, индивидуально им присущей буферной способностью (см. п. 6.1.1).[ ...]
Крайняя кривая (верхний правый угол рисунка) относится к МпБ при pH« 8, при меньших pH это вещество более растворимо. При выбранных масштабах аналогичные кривые для меди практически бы совпали с осями.[ ...]
Кремний как х-имический элемент занимает второе место по содержанию в литосфере нашей планеты. В пресных водах его концентрация варьирует в пределах 0,1—4000 млн-1, при этом в большинстве озер эти пределы оказываются более узкими, 2—25 млн-1 (в литературе обычно упоминается как двуокись кремния, БЮг).[ ...]
Присутствие растворенной двуокиси кремния в водоемах является существенным для диатомовых водорослей, для построения ими панциря (в основе «строительного» материала которого лежит кремний). В летний период, когда исчезают диатомовые, накопленный в них кремний медленно возвращается в водную среду. Часть его оказывается захороненной в бентосных иловых отложениях.[ ...]
Приведенные в табл. 6.6 характерные концентрации кремния в поверхностных водах дают основание предположить, что в озерах более низких (тропических) широт содержание кремния может быть еще выше.[ ...]
Максимальной концентрации БЮг, приведенной на этом рисунке, соответствует значение 2,5 мг/л.[ ...]
Пути поступлений и стоков кремния в водоеме, в отличие от многих других биогенных элементов (таких, как N и Р), не отличаются особой сложностью. Включение же кремниевого цикла в полную модель эвтрофикации представляется весьма желательным.[ ...]
Направление движения электронов указывает на характер тестируемой жидкости с точки зрения ее способности к окислению или восстановлению. Согласно сказанному выше, окислители и восстановители должны иметь потенциалы соответственно больше или меньше нуля.[ ...]
В щелочной и окислительной средах соединения железа осаждаются; при pH, равном 7,5—7,7, осаждается гидрат окиси железа Ре(ОН)з. Из сказанного следует, что железо в растворенном состоянии характерно для вод от кислых до нейтральных, обедненных кислородом, с восстановительно-окислительным потенциалом от 0,3 до 0,2. Такие воды в свою очередь характерны для эвтроф-ных озер в области гиполимниона. Однако увеличение концентрации растворенного кислорода в придонных слоях вследствие перемешивания приводит к окислению железа и его последующему осаждению.[ ...]
Рисунки к данной главе:
| Кривые растворимости РеБ, рассчитанные для различных pH воды [244]. |
![Кривые растворимости РеБ, рассчитанные для различных pH воды [244].](/static/pngsmall/901285292.png) |
| Связь между концентрацией растворимого кремния (заштрихованная область) и колебаниями концентрации диатомовых сообществ (сплошная линия) [83, 328]. |
![Связь между концентрацией растворимого кремния (заштрихованная область) и колебаниями концентрации диатомовых сообществ (сплошная линия) [83, 328].](/static/pngsmall/901285294.png) |
| Модельное представление важнейших элементов круговорота железа в озере с аноксическим гиполимнионом [103]. |
![Модельное представление важнейших элементов круговорота железа в озере с аноксическим гиполимнионом [103].](/static/pngsmall/901285300.png) |
| Иллюстративное представление простой модели круговорота железа и |
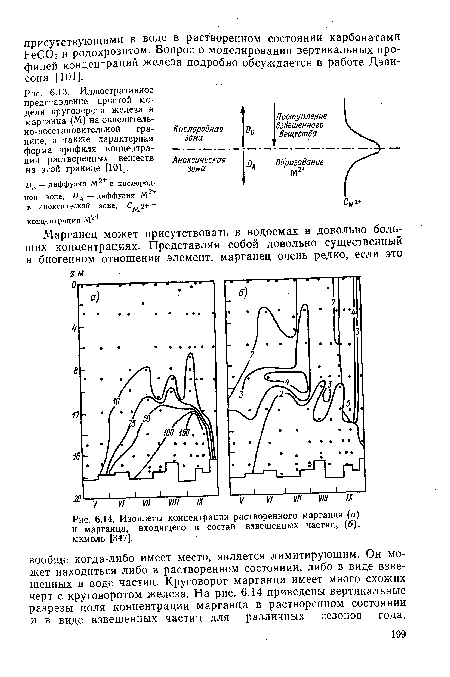 |
| Изоплеты концентрации растворенного марганца (о) и марганца, входящего в состав взвешенных частиц, (б), мкмоль [347]. |
![Изоплеты концентрации растворенного марганца (о) и марганца, входящего в состав взвешенных частиц, (б), мкмоль [347].](/static/pngsmall/901285302.png) |