В системах оборотного (а также прямоточного) водоснабжения металлы разрушаются от коррозии вследствие физико-хи-мического взаимодействия их с окружающей средой. В системах водоснабжения применяют в основном простые металлы (сталь, чугун), а также изделия и оборудование, изготовленные из этих металлов; средой, в которой происходит коррозия металлов, является вода. Следовательно, процессы коррозии связаны с характерными особенностями воды и металла. Однако коррозию следует отличать от эрозии — поверхностного механического разрушения металлов.[ ...]
По условиям протекания коррозию в системах водоснабжения делят на электрохимическую и биологическую.[ ...]
Электрохимическая коррозия представляет собой два одновременно происходящих процесса: окислительный (растворение металла на одном участке — аноде) и восстановительный (выделение катиона из раствора и восстановление кислорода на другом участке — катоде). На одном и том же участке металлической поверхности могут проходить одновременно анодный и катодный процессы.[ ...]
Нередко в системах оборотного водоснабжения наблюдают биологическую коррозию при участии продуктов, выделяемых микроорганизмами биологических обрастаний.[ ...]
В отдельных случаях возникает коррозия при трении (коррозионная эрозия) — разрушение металла, вызываемое одновременно воздействием коррозионной среды и трением (например, разрушение шеек валков прокатных станов, охлаждаемых морской водой).[ ...]
По характеру разрушений коррозия может быть сплошной и местной. Сплошная или общая коррозия бывает равномерной (протекающая примерно с одинаковой скоростью по всей поверхности металла) и неравномерной (протекающая с неодинаковой скоростью на различных участках поверхности металла). Местная коррозия может быть в виде отдельных пятен и язв (см. рис. 174) или в виде отдельных точек (до сквозных).[ ...]
Не рассматривая сущности теории и процессов коррозии, отметим, что существует ряд факторов, ускоряющих или замедляющих коррозию металлических труб, аппаратов и другого оборудования систем водоснабжения.[ ...]
Влияние температуры на скорость коррозии стали не одинаковое: в закрытой системе водоснабжения с увеличением температуры воды коррозия усиливается, что объясняется торможением свободного выделения кислорода из воды; в открытой системе оборотного водоснабжения коррозия усиливается до температуры 70—80° С, после чего наступает снижение коррозии вследствие сильного уменьшения растворимости кислорода с повышением температуры.[ ...]
Углекислота сама по себе не вызывает сильной коррозии при щелочных и нейтральных водах; при концентрации в воде С02своб ДО 30 мг/л скорость коррозии углеродистой стали остается почти такой же, что и в воде, не содержащей углекислоты, затем она возрастает и превосходит допустимый предел при концентрации С02(;во6 свыше 70 мг/л. Это явление можно объяснить тем, что свободная углекислота, способствуя удержанию в растворе солей кальция, препятствует образованию защитной пленки. В оборотной охлаждающей воде свободной углекислоты содержится 3—4 мг/л, при рекарбонизации может быть до 50— 70 мг/л.[ ...]
При содержании хлор-иона в оборотной охлаждающей воде до 100—150 мг/л воду можно считать слабо агрессивной, с возрастанием концентрации агрессивность воды увеличивается.[ ...]
Рисунки к данной главе:
| Коррозия металла |
 |
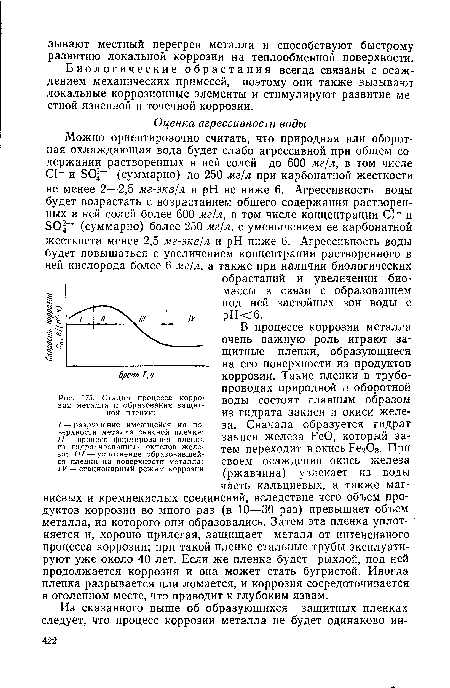
| Стадии процесса коррозии металла и образования защитной пленки |
 |
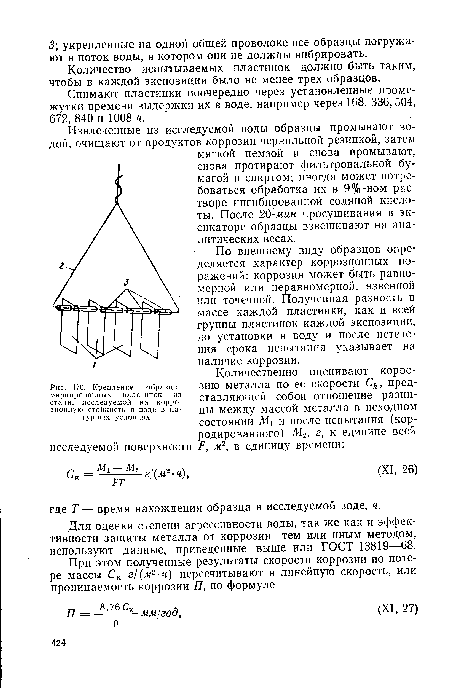
| Крепление образцов маркированных пластинок из стали, исследуемой на коррозионную стойкость в воде в натурных условиях |
 |