Химические реакции, служащие для количественных определений отдельных составных частей анализируемого материала, проводят обычно в растворах. Все водные растворы, применяемые в анализе, готовятся на дистиллированной воде. Концентрация растворов выражается различными способами.[ ...]
Процентная концентрация выражается в весовых процентах, то есть в граммах растворенного вещества, содержащегося в 100 г раствора.[ ...]
Нормальная концентрация выражается числом грамм-эквивалентов (или миллиграмм-эквивалентов) растворенного вещества, содержащегося в 1 л раствора.[ ...]
При приготовлении нормальных растворов следует иметь в виду, что эквивалент одного и того же вещества может быть различным по величине, что зависит от вида химической реакции, в которой должно участвовать растворенное вещество.[ ...]
Растворы, служащие для проведения количественных химических реакций, когда требуется знать точное количество реактива, пошедшего на реакцию с определяемым веществом, называются точными, или титрованными, растворами. Относительная ошибка при их приготовлении не должна превышать 0,1%.[ ...]
Кроме титрованных растворов, в анализе применяют приблизительные растворы, концентрация которых выражается со значительно меньшей точностью. Такими растворами часто пользуются для извлечения составных частей из анализируемого материала, осаждения этих составных частей, создания определенных условий течения химических реакций и для многих других целей.[ ...]
Приблизительные растворы жидких кислот, а также растворы аммиака, спирта готовят на основании определения удельного веса этих жидкостей. Наиболее быстро удельный вес определяется ареометрами. При этом жидкость наливают в чистый совершенно сухой цилиндр емкостью не менее 0,5 л;. полностью цилиндр не заполняют — должен остаться свободный объем, по крайней мере в 2 раза превышающий объем ареометра. Высота столба жидкости в цилиндре после погружения ареометра должна быть не меньше полной его высоты. Ареометр перед погружением тщательно моют и высушивают. Чтобы избежать ошибки вследствие мениска, ареометр при отсчете по шкале не должен находиться близко к стенке. После определения плотности ареометр обмывают водой, вытирают и убирают в футляр.[ ...]
На основании определения удельного веса жидкости находят по таблице концентрацию данного вещества.[ ...]
Пример 1. Требуется приготовить 1 л 25%-ного раствора серной кислоты. Плотность исходной кислоты при 19° равна 1,8365.[ ...]
Рассчитаем сначала, сколько чистой (100%-ной) серной кислоты требуется для приготовления 1 л 25%-ного раствора? Находим по таблице удельных весов, что 25%-ный раствор при 20° имеет плотность 1,178; следовательно, 1 л раствора весит 1178 г.[ ...]
Рисунки к данной главе:
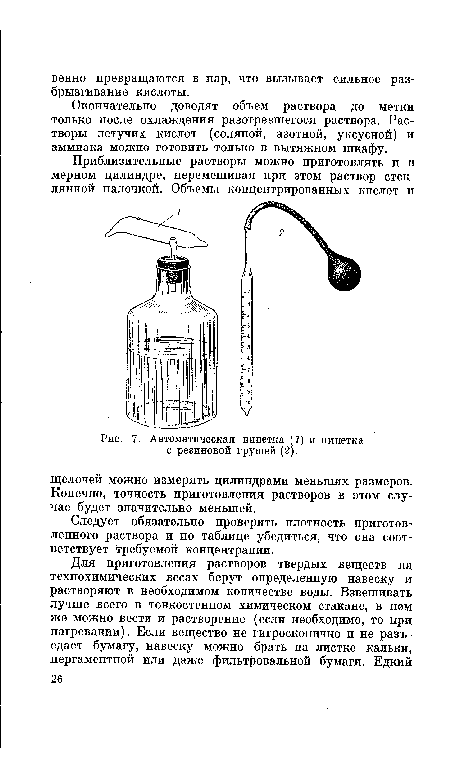
| Автоматическая пипетка (1) и пипетка с резиновой грушей (2). |
 |
Аналогичные главы в дргуих документах:
| См. далее:Приготовление растворов |