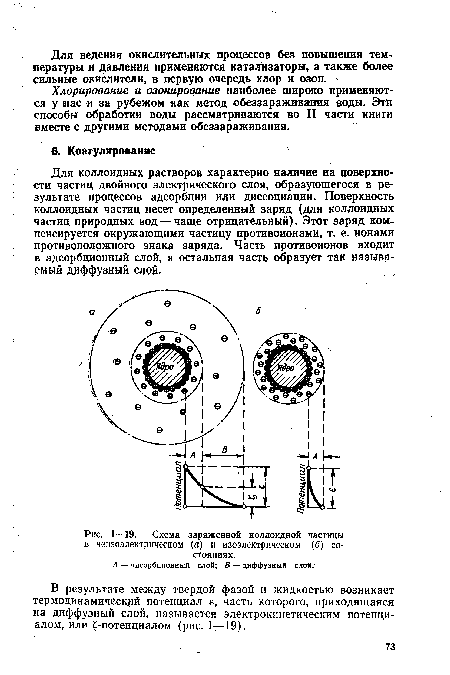
Для коллоидных растворов характерно наличие на поверхности частиц двойного электрического слоя, образующегося в результате процессов адсорбции или диссоциации. Поверхность коллоидных частиц несет определенный заряд (для коллоидных частиц природных вод — чаще отрицательный). Этот заряд компенсируется окружающими частицу противоионами, т. е. ионами противоположного знака заряда. Часть противоионов входит в адсорбционный слой, а остальная часть образует так называемый диффузный слой.[ ...]
А — адсорбционный слой; В — диффузный слой.[ ...]
В результате между твердой фазой и жидкостью возникает термодинамический потенциал е, часть которого, приходящаяся на диффузный слой, называется электрокинетическим потенциалом, или -потенциалом (рис. 1—19).[ ...]
Наибольшее развитие диффузный слой получает при очень малых концентрациях электролита в растворе. Причиной этого является тепловое движение ионов, под действием которого они стремятся равномерно распределиться во всем объеме жидкости. В этом случае С-потенциал достигает максимальных значений. Напротив, при добавлении электролитов концентрация ионов в диффузном слое увеличивается, и для компенсации зарядов на поверхности частиц потребуется меньший объем диффузного слоя, т. е. наблюдается его сжатие. Одновременно происходит переход части противононов в адсорбционный слой и С-потенциал уменьшается.[ ...]
При снижении величины С-потенциала до ±30 мв начинается коагуляция.[ ...]
Коагуляция в принципе может быть вызвана добавлением любых ионов, имеющих заряд, противоположный по знаку заряду поверхности коллоидной частицы, однако коагулирующее действие резко усиливается с увеличением валентности ионов (согласно правилу Шульце-Гарди, коагулирующая сила одно-, двух- и трехвалентных ионов находится в примерном соотношении 1:20:400). Для ионов одной и той же валентности коагулирующее действие усиливается при увеличении радиуса ионов, например, для одновалентных ионов—от лития к цезию (Воюцкий, 1964).[ ...]
Применительно к очистке сточных вод коагулирование — процесс укрупнения присутствующих в стоках взвешенных и коллоидных частиц и выпадения их в осадок.[ ...]
Анионы алюмосиликата образуют основу отрицательно заряженной глинистой частицы, окруженной сферой положительных компенсирующих ионов водорода. При подкислении среды уменьшается степень диссоциации слабой алюмосиликатной кислоты и, следовательно, количество ионов, находящихся в диффузном слое. Глинистая взвесь коагулирует. Напротиз, подщелачивание придает глинистой взвеси повышенную устойчивость. Вызвать коагуляцию можно в данном случае добавлением положительно заряженных ионов. Зависимость устойчивости дисперсной системы от величины -потенциала частиц характерна для гидрофобных коллоидов. Однако в практике очистки природных и сточных вод нередко приходится иметь дело с коллоидами гидрофильными, которые не только менее чувствительны к добавлению электролитов, но и способны оказывать защитное действие по отношению к гидрофобным коллоидам.[ ...]
Разрушение защитных коллоидов обычно может быть достигнуто окислением органических веществ хлором или другими окислителями.[ ...]
Рисунки к данной главе:
| Схема заряженной коллоидной частицы в неизоэлектрическом (а) и изоэлектрическом (б) состояниях. |
 |
Аналогичные главы в дргуих документах:
| См. далее:Коагулирование |