Природные, сточные и другие виды вод представляют собой сложные системы, основу которых составляет химическое соединение, имеющее простую формулу Н20. На первый взгляд, за этой формулой стоит ничем не примечательное соединение. При более глубоком ознакомлении со строением молекулы и свойствами воды выясняется, что она обладает рядом удивительных свойств.[ ...]
Молекула воды состоит из двух атомов водорода и одного атома кислорода.[ ...]
Для состава воды характерно следующее массовое содержание элементов (%): водорода 11,19 и кислорода 88,81. Ядра атомов в молекуле воды расположены по углам равнобедренного треугольника, в вершине которого находится ядро атома кислорода. Молекула воды — плоская угловая. В невозбужденных молекулах воды угол НОН, образованный направлениями связей кислород — водород, составляет 104°27/ (для парообразного состояния) и 104°ЗГ (для жидкого) (рис. 1).[ ...]
Межъядерное расстояние О—Н в молекулах воды равно 0,09568 нм (в газовой фазе), 0,09572 нм (в жидкой) и 0,099 нм (в фазе льда). Колебательное, вращательное и электронное возбуждение молекул воды вызывает изменение размеров и формы молекулы Н20. Причем энергетически выгодной является одновременная деформация угла и длины связи О—Н.[ ...]
Таким образом, электронное облако молекулы воды имеет вид четырех лепестков, направленных к вершинам неправильного тетраэдра. В двух вершинах одной грани находятся электронные пары, осуществляющие связь О—Н, а в двух вершинах противоположной грани находятся неподеленные электронные пары атома кислорода (рис. 2). Электронное облако в молекуле воды смещается к атому кислорода, так как он имеет большую электроотрицательность. Вследствие этого вблизи ядер атомов водорода создается избыток положительного заряда. Поэтому молекула воды поляр-на. Полярные молекулы характеризуются электрическим моментом диполя, который влияет на свойства веществ, состоящих из таких молекул. Электрический момент диполя представляет собой произведение одного из зарядов на расстояние между центрами положительного и отрицательного заряда I. Для воды электрический момент диполя р = е1 равен 6-10 28 Кл-м. Благодаря большому значению электрического момента диполя между молекулами воды проявляется сильное взаимодействие за счет образования водородных связей между атомом кислорода одной молекулы воды и атомом водорода другой.[ ...]
Рассмотрим структуру воды в различных агрегатных состояниях. При 0° С (273,15 К) жидкая вода превращается в лед. Средняя величина электрического момента диполя у молекулы воды в упорядоченной структуре льда составляет 8,58-10-’28. Плотность льда при 0°С 0,9168 г/см3.[ ...]
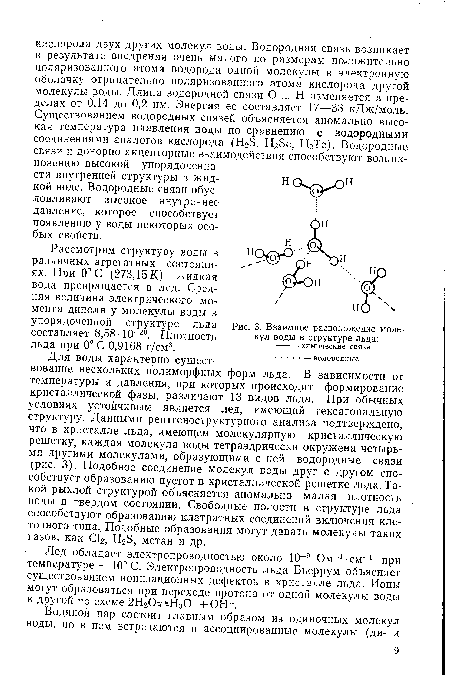
Для воды характерно существование нескольких полиморфных форм льда. В зависимости от температуры и давления, при которых происходит формирование кристаллической фазы, различают 13 видов льда. При обычных условиях устойчивым является лед, имеющий гексагональную структуру. Данными рентгеноструктурного анализа подтверждено, что в кристалле льда, имеющем молекулярную кристаллическую решетку, каждая молекула воды тетраэдрически окружена четырьмя другими молекулами, образующими с ней водородные связи (рис. 3). Подобное соединение молекул воды друг с другом способствует образованию пустот в кристаллической решетке льда. Такой рыхлой структурой объясняется аномально малая плотность воды в твердом состоянии. Свободные полости в структуре льда способствуют образованию клатратных соединений включения клеточного типа. Подобные образования могут давать молекулы таких газов, как С12, Н2Э, метан и др.[ ...]
Лед обладает электропроводностью около 10 9 Ом -см“1 при температуре —10° С. Электропроводность льда Бьеррум объясняет существованием ионизационных дефектов в кристалле льда. Ионы могут образоваться при переходе протона от одной молекулы воды к другой по схеме 2Н20 Н30++0Н .[ ...]
Многие ученые придерживаются теории строения жидкой воды и водных растворов, в основе которой лежит положение о сохранении ажурной решетки льда в жидкой воде и частичном заполнении пустот одиночными молекулами воды. По этой теории ближняя упорядоченность молекул воды, т. е. взаимное расположение соседних молекул воды, аналогично кристаллическому каркасу льда, слегка нарушенному тепловым движением молекул, в пустотах которого находятся одиночные молекулы воды.[ ...]
О. Я. Самойловым разработана теория трансляционного движения частиц в воде, согласно которой молекулы воды льдоподобного каркаса, выйдя из состояния равновесия, совершают активированный скачок в пустоты, находятся там некоторое время, а затем вновь приходят в трансляционное движение. Молекулы воды, попавшие в пустоты, энергетически не соответствуют молекулам каркаса. Время перехода молекул воды из одного состояния в другое составляет порядка 10-13 с.[ ...]
Рисунки к данной главе:
| Строение молекулы воды |
 |
| Направленность электронных орбиталей (а) и схема распределения зарядов в молекуле воды (б) |
 |
| Взаимное расположение молекул воды в структуре льда |
 |
Аналогичные главы в дргуих документах:
| См. далее:Вода как химическое соединение |