Как отмечалось в разд. 8.3, количество N0 и N02, образующееся в различных системах сжигания, не находит удовлетворительного объяснения на основе лишь одного термодинамического анализа. Необходимо также принять во внимание скорость реакции. Применение химической кинетики к процессам горения с участием атмосферных азота и кислорода помогло выяснить структуру системы химических реакций, которая приводит к образованию окислов азота. Хотя в целом механизм реакций очень сложен и некоторые его детали еще остаются спорными, с середины 60-х годов был достигнут значительный успех в понимании сложных химических процессов.[ ...]
Однако реакции (8.4) и (8.5), безусловно, являются наиболее важными для образования N0 в бедном и средпеобогащенном топливом пламени (ф 1,2). Реакция (8.6) имеет некоторое значение для обогащенного топливом пламени при ср>1,2, где <р — эквивалентное соотношение смеси топлива с воздухом. Реакция (8.4) обычно является реакцией, определяющей скорость, поскольку разрыв связи в N2 — наиболее трудная стадия в механизме Зельдовича.[ ...]
На основе элементарных реакций можно вывести уравнение для расчета скорости образования окиси азота. Чрезвычайно важно при этом, однако, четко представлять себе механизм и исходные посылки. Скорости, основанные на разных механизмах газофазного горения, могут существенно отличаться. Эти различия в скоростях образования N0 могут быть прямо связаны с концентрацией атомов О и с температурными зависимостями, рассчитанными для различных механизмов горения [26].[ ...]
Основным подходом к расчету скоростей образования NO, во-первых, является ограничение протекания реакций (8.4) и (8.5), т. е.[ ...]
Теперь нам предстоит выразить некоторые члены в правой части уравнения с учетом других переменных.[ ...]
Это один из возможных видов уравнения скорости образования окиси азота из атмосферного азота в процессах горения.[ ...]
Значение каждого члена в правой части уравнения (8.12) обычно известно.[ ...]
Это уравнение связывает количество образующейся N0(7) со временем t с учетом параметров С и М.[ ...]
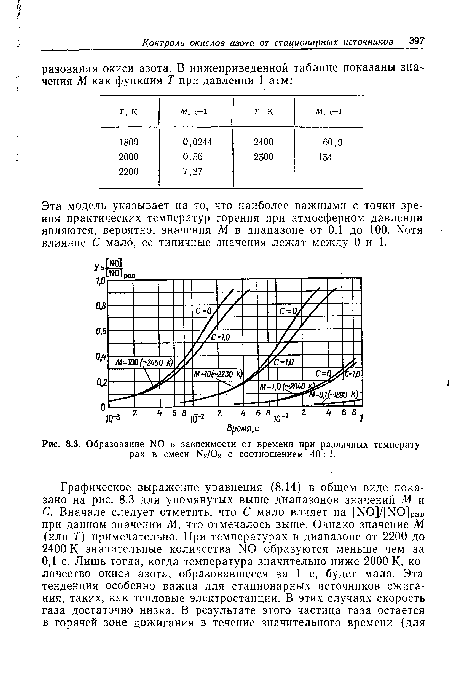
Эта модель указывает на то, что наиболее важными с точки зрения практических температур горения при атмосферном давлении являются, вероятно, значения М в диапазоне от 0,1 до 100. Хотя влияние С мало, ее типичные значения лежат между 0 и 1.[ ...]
Предположение о фиксированной температуре было сделано для получения обобщенных кривых, показанных на рис. 8.3 и 8.4. На практике же температура, конечно, может падать в результате теплопередачи или эффекта разбавления. В результате истинное конечное содержание N0 сильно зависит от температурного и временного режимов в зоне дожигания. Влияние начального состава в зоне дожигания уже обсуждалось. Тем не менее в предшествующей дискуссии были изложены некоторые из основных или основополагающих причин образования N0 в процессах горения с участием атмосферного воздуха. Методы контроля над процессами сжигания основаны на понимании основных факторов.[ ...]
Рисунки к данной главе:
| Образование N0 в зависимости от времени при различных температурах в смеси N2/02 с соотношением 40 |
 |
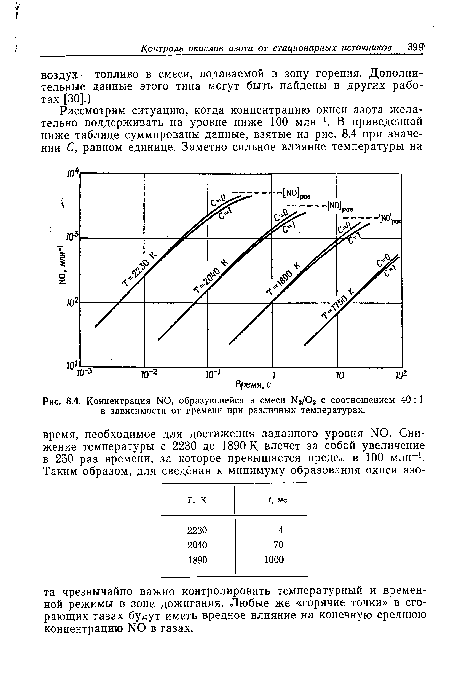
| Концентрация N0, образующейся в смеси Ы2/02 с соотношением 40 |
 |