При содержании С02 в атмосфере, равном 340 млн 1 , и при температуре 20 °С расчетная концентрация ионов водорода составляет 2,3 ■ 10 6 г-ион/л, что соответствует pH = 5,6. Поэтому "кислотными" принято называть атмосферные осадки с водородным показателем ниже этого значения.[ ...]
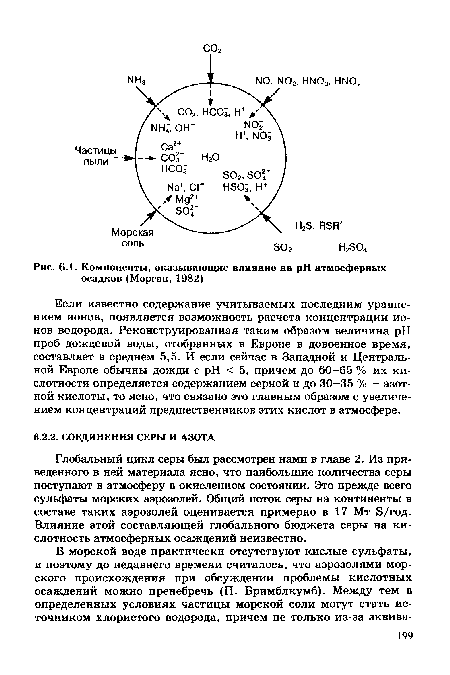
Реально водородный показатель дождевой воды, отобранной в разных районах мира, лежит в пределах 2 < pH < 9. "Раскисление" происходит обычно при захвате каплями дождя некоторых видов аэрозолей - частиц карбонатных пород или морских аэрозолей (морская вода в силу своего ионного состава имеет щелочную реакцию, что отражается на составе образующихся из нее аэрозолей). На рис. 6.1 показаны компоненты, определяющие значения pH осадков.[ ...]
Если известно содержание учитываемых последним уравнением ионов, появляется возможность расчета концентрации ионов водорода. Реконструированная таким образом величина pH проб дождевой воды, отобранных в Европе в довоенное время, составляет в среднем 5,5. И если сейчас в Западной и Центральной Европе обычны дожди с pH < 5, причем до 60-65 % их кислотности определяется содержанием серной и до 30-35 % - азотной кислоты, то ясно, что связано это главным образом с увеличением концентраций предшественников этих кислот в атмосфере.[ ...]
Рисунки к данной главе:
| Компоненты, оказывающие влияние на pH атмосферных осадков (Морган, 1982) |
 |