На практике исследования состава окрашенных промышленных сточных вод удобно пользоваться электрометрическими методами титрования — это потенциометрическое титрование и кондуктомет-рическое титрование.[ ...]
Потенциометрическое титрование основано на линейной зависимости между электродным потенциалом и показателем концентрации ионов в растворе. Если применяемый при титровании электрод обратим по отношению к ионам титруемого или титрующего вещества, то изменение потенциала такого электрода во время титрования указывает на изменение концентрации ионов в растворе.[ ...]
Потенциометрическое титрование, как и обычное, основано на резком изменении вблизи эквивалентной точки концентрации титруемого вещества при добавлении к последнему небольшого количества титрованного раствора.[ ...]
Точные результаты могут быть получены: 1) ;при титровании сильных кислот сильными основаниями и наоборот; 2) при титровании слабых кислот сильными основаниями и наоборот (если константа диссоциации не ниже 1- 10 8); 3) при титровании смссн кислот примерно равных концентраций, но различных по величине-констант диссоциации не менее чем в 100 раз; 4) ¡при титровании многоосновных кислот, если отношение констант диссоциации /Сх:/Сп=Ю4.[ ...]
Определение концентрации вещества по методу потенциометрического титрования сводится к измерению потенциала индикаторного электрода на потенциометре в процессе нейтрализации раствора и к построению кривой титрования.[ ...]
Кривая титрования смеси двух -кислот отвечает двум точкам перегиба — первый перегиб отвечает точке нейтрализации сильной кислоты, а второй — слабой, как показано на рис. 18. Если перегибы на кривой титрования расплывчаты, то для выявления резкого скачка результаты титрования представляют в виде дифференциальной кривой рис. 19. Вершины кривой соответствуют точкам эквивалентности.[ ...]
Кондуктометрическое титрование. Метод кондуктометрическогп титрования основан на измерении удельной электропроводности растворов. Характер изменения электропроводности при титровании зависит от природы добавляемых ионов, т. е. от их подвижности, а также от образования малодиссоциированных веществ.[ ...]
Экспериментальные кривые изменения удельной электропроводности в зависимости от количества миллилитров добавленного титрованного раствора называют кондуктометрическими. Положение точки эквивалентности определяют изломом кривой, так как избыток реагента после точки эквивалентности приводит к увеличению электропроводности.[ ...]
Кондуктометрическим титрованием можно определять концентрации смеси кислот различной силы. При этом на кривых титрования получается столько перегибов, сколько в растворе кислот (рис. 21).[ ...]
Первый перегиб дает точку эквивалентности (Ь), соответствующую количеству более сильной кислоты, последующие перегибы расположены в порядке убыли силы кислоты.[ ...]
Рисунки к данной главе:
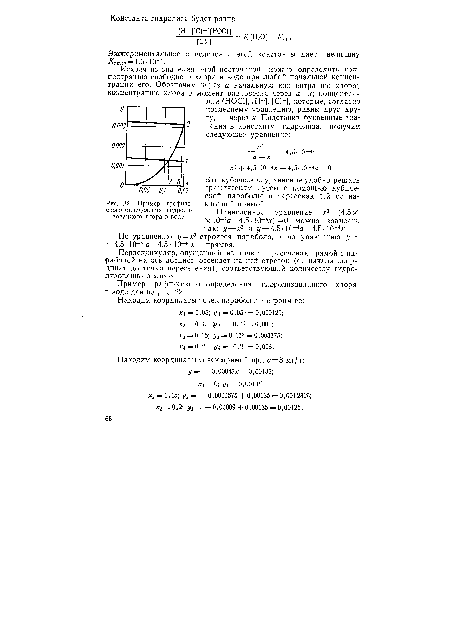
| Пример графического определения гидролизованного хлора в воде |
 |