При оценке закономерностей процессов, протекающих на соору- жениях очистки природных и сточных вод, часто пользуются методами химической кинетики, определяющими порядок реакции.[ ...]
По реакции 1-го порядка протекают такие химические процессы, когда одно из веществ изменяет свою концентрацию, а изменение концентрации второго происходит незаметно из-за его большой концентрации, например гидролиз солей.[ ...]
Общий порядок реакции определяется суммой (а- -Ь). Частные порядки реакций определяются одним из рассматриваемых методов.[ ...]
В практике очистки природных и сточных вод приходится сталкиваться с целым комплексом химических процессов, направленность которых можно заранее определить расчетным путем по изменению термодинамических потенциалов участвующих компонентов. Наиболее удобными для подобных расчетов являются изобарно-изометрический О п изохорно-нзотермический (Т7) потенциалы. Изохорно-изотермический потенциал служит для определения направления и предела течения самопроизвольных процессов в неизолированной системе (при V, 7 = сопз1). Изобарно-изотермический потенциал характеризует те же процессы при постоянном давлении и постоянной температуре.[ ...]
Термодинамические потенциалы — термодинамические функции, не зависящие от пути перехода процесса, а только от начального и конечного состояния участвующих в реакции веществ.[ ...]
Величины А/7 и АО характеризуют соответственно свободную энергию при .постоянном объеме и постоянном давлении, которая в обратимом изотермическом процессе может быть превращена в работу.[ ...]
Произведение температуры на энтропию (ТБ) называют связанной энергией. Это та энергия, которая не может быть превращена в работу.[ ...]
Следовательно, изменение термодинамических потенциалов равно максимальной полезной работе, взятой с обратным знаком. Нели АР или ДС=0, то система находится в термодинамическом равновесии. Самопроизвольно будут протекать только те процессы, у которых АР или ДО будут меньше нуля.[ ...]
Итак, возможность, направление и предел течения изобарно-или изохорно-нзотермнческого процессов в неизолированной системе определяется знаком разности Д(3 = 02—а термодинамические возможности этого процесса — абсолютной величиной этой разности.[ ...]
Рисунки к данной главе:
| Изменение функций концентрации исходных веществ но времени для реакций различных порядков |
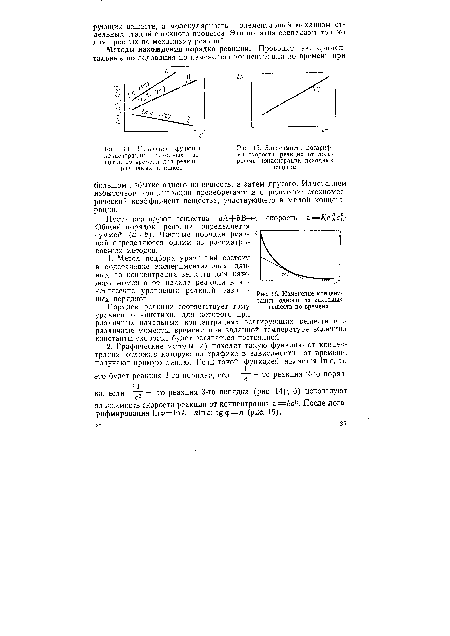 |
| Зависимость логарифма скорости реакции от логарифма концентрации исходных веществ |
 |